Оксиазосоединение
Cтраница 1
Оксиазосоединения и аминоазосоелинения являются бензоидными формами, таутомерными с гидразонами хинонов и хинонимидов. [1]
Оксиазосоединения, содержащие одну или несколько гидроксильных групп в одном ядре, полученные, например, из диазотированного я-нитроанилина и фенола, 1 2-и 1 3-диокси-бензола, 1 3-диокси - 5-метилбензола, 1 2 3 - и 1 3 5-трпоксибен-зола, я - и [ 3-нафтола и их сульфокислот, не реагируют с борной кислотой. [2]
Оксиазосоединения, содержащие одну или несколько гидроксильных групп в одном ядре, полученные, например, цз диазотированного н-нитроанилина и фенола, 1 2 - и 1 3-диоксп-бензола, 1 3-диокси - 5-метилбензола, 1 2 3 - и 1 3 5-триоксибен-зола, ос - и ( 3-нафтола и их сульфокислот, не реагируют с борной кислотой. [3]
Оксиазосоединения меркурируются уксуснокислой ртутью в водном, спиртовом или слабоуксуснокислом растворе при более продолжительном ( до 7 час. [4]
Образование оксиазосоединений в результате взаимодействия солей диазония с фенолами уже было рассмотрено ранее ( см. стр. [5]
Для оксиазосоединений также характерна нерастворимость или малая растворимость в щелочах. [6]
Аминоазосоединения и оксиазосоединения обычно получают взаимодействием ароматических диазосоединений с аминами и фенолами ( стр. Эта реакция называется реакцией сочетания или азосочетания. [7]
Аминоазосоединения и оксиазосоединения обычно получают взаимодействием ароматических диазосоединений с аминами и фенолами ( стр. [8]
Итак, оксиазосоединения представляют пример тавтомерии, каковая встречается в области органических красителей весьма часто. [9]
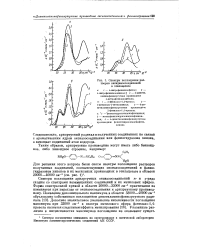 |
Спектры поглощения растворов оксидиазосоединений в этилацетате. [10] |
Спектры поглощения арилртутных оксиазосоединений п - и о-ряда сходны со спектрами незамещенных соединений и их метиловых эфиров. Форма спектральной кривой в области 20000 - 33000 см-1 практически не изменяется при переходе от оксиазосоединения к арилртутному производному. [11]
Следовательно, арилртутные производные оксиазосоединений и в твердом состоянии имеют бензоидное строение, а производные фенилгидразонов хинонов обладают хинонгидразонной структурой. [12]
Интересно, что оксиазосоединения с двумя или большим числом сульфогрупп не дают экстрагирующихся комплексов. [13]
А), восстановлением оксиазосоединений ( способ Б), сплавлением наф-тиламинсульфокислот с едким натром ( способ В, промышленный), действием амида натрия на нафтолы ( способ Г), отщеплением сульфогруппы от амиионафтол-судьфокислоты при нагревании с разбавленной к-той ( способ Д) или при действии амальгамы натрия ( способ Е), действием аммиака на диоксинафталины при высокой темп-ре ( способ Ж), действием бисульфита натрия на нафтилендиамины ( способ 3) и др. В пром-сти применяют лишь 1 5 -, 1 7 - и 1 8 - А. [14]
А), восстановлением оксиазосоединений ( способ В), сплавлением наф-тиламинсульфокислот с едким натром ( способ В, промышленный), действием амида натрия на нафтолы ( способ Г), отщеплением сульфогруппы от аминонафтол-сульфокислоты при нагревании с разбавленной к-той ( способ Д) или при действии амальгамы натрия ( способ Е), действием аммиака на диоксинафталины при высокой темп-ре ( способ Ж), действием бисульфита натрия на нафтилендиамшш ( способ 3) и др. В пром-сти применяют лишь 1 5 -, 1 7 - и 1 8 - А. [15]
Страницы: 1 2 3