Оксибутират
Cтраница 2
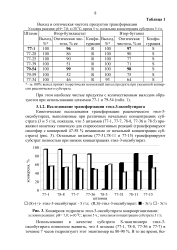 |
Конверсия гидролиза этил-3 - оксибутирата микроорганизмами. [16] |
Остальные штаммы ( 77 - 31 78 - 11 и 77 - 15) трансформируют субстрат полностью при низких концентрациях этил-3 - оксибутират. [17]
Ранее нами были найдены микроорганизмы, клетки ( или обезвоженные ацетоном клетки) которых способны эффективно осуществлять стереоселективный гидролиз рацемических смесей вторичного бутилацетата, этил-3 - оксибутирата и / или парциальное ацилирование ( К 8) - гептанола-2 винилацетатом с образованием энантиомерных соединений высокой оптической чистоты и выходом близким к теоретически возможному. На данном этапе проведено исследование дополнительных каталитических возможностей найденных биокатализаторов с целью разработки новых методов стереоселективного разделения рацемических смесей аминов и спиртов с помощью клеток микроорганизмов. [18]
В качестве трансформируемого субстрата был использован этилацетоацетат ( ЭАА), оптически активные продукты восстановления которого, S-этил - З - оксибутират ( S-ЭОБ) и R-этил - З - оксибутират ( R-ЭОБ), применяются в синтезе феромонов насекомых, используемых для защиты сельскохозяйственных культур, синтезе шовных материалов для хирургии, биоразлагаемых полимеров, практически ценных биорегуляторов ( карбомицина В, RR-пиренофорина, грамицина А, сулькатола, коллетодиола и ресифеолида), а также материалов-антиоксидантов для пищевой промышленности. [19]
Объектами исследования являлись микроорганизмы, полученные на предыдущем этапе работы [2,3], клетки которых в стандартных условиях осуществляли стереоселективный гидролиз рацемических смесей втор-бутилацетата ( штамм 79 - 54), этил-3 - оксибутирата ( штамм 78 - 5), а также парциальное ацилирование гептанола-2 винилацетатом ( штаммы 77 - 47 и 77 - 33) с образованием энантиомерных соединений высокой оптической чистоты и выходом, близким к теоретическому. [20]
Созданы препаративные методы получения ( S) - () - втор-бутанола, ( К) - ( -) - втор-бутилацетата, ( 8) - () - этил-3 - оксибутирата, ( R) - ( -) - этил-3 - оксибутирата, ( 8) - () - 3-оксимасляной кислоты, ( К) - ( -) - 3-оксимасляной кислоты, ( S) - () - глицидола и ( К) - ( -) - глицидола высокой оптической чистоты ( 96 - 100 % ее), которые являются ценными синтонами при получении различных низкомолекулярных биорегуляторов ( феромонов насекомых, ( 3-адренергетиков, цереброзидов, гормонов, простагландинов, нуклеозидов) и биоразлагаемых полимеров. [21]
Объектами биотрансформации являлись липолитические микроорганизмы синтезирующие внеклеточные или внутриклеточные липазы, выделенные из почвенных образцов, взятых с различных участков химических производств Республики Башкортостан и Сибири, а также втор-бутилацетат, этил-3 - оксибутират, глицидиловый эфир метакриловой кислоты и М - ЗЕ-пентен-2-ил-ортотолуидин ацетамид. [22]
В результате сравнительного анализа принципиальных схем разделения в водной ( рис. 5) и в органической ( рис. 6) средах установлено, что получение оптически активных остаточных субстратов - втор-бутилацетата и этил-3 - оксибутирата предпочтительнее проводить в гексане вследствие меньшей трудоемкости и большей эффективности разделения. [23]
Созданы препаративные методы получения ( S) - () - втор-бутанола, ( К) - ( -) - втор-бутилацетата, ( 8) - () - этил-3 - оксибутирата, ( R) - ( -) - этил-3 - оксибутирата, ( 8) - () - 3-оксимасляной кислоты, ( К) - ( -) - 3-оксимасляной кислоты, ( S) - () - глицидола и ( К) - ( -) - глицидола высокой оптической чистоты ( 96 - 100 % ее), которые являются ценными синтонами при получении различных низкомолекулярных биорегуляторов ( феромонов насекомых, ( 3-адренергетиков, цереброзидов, гормонов, простагландинов, нуклеозидов) и биоразлагаемых полимеров. [24]
Найдены оптимальные параметры энантиоселективного гидролиза ( температура 30 - 35 С; рН7 5 - 8 0; начальная концентрация субстрата 5 - 7 г / л; концентрация сорастворителя 30 - 35 % об. в зависимости от типа штамма) втор-бутилацетата и этил-3 - оксибутирата для полученных биокатализаторов. [25]
Сравнение модифицирующих свойств L - ap - треонина и L - aa - ал-лотреонина показало различие полученных катализаторов. Обработка Ь - о р-аллотреонином при 0 С дает преимущественно L - () - оксибутират, с увеличением температуры модифицирования резко возрастает доля D-изомера. [26]
Важно подчеркнуть, что, например, при голодании адаптация метаболических превращений направлена на сведение к минимуму расщепления белка и аминокислот. При этом в печени из ацетил - КоА активируется синтез кетоновых тел ( Р - оксибутирата и ацетона), которые служат источником энергии для многих тканей, в том числе и мозга. Это приводит к уменьшению скорости распада белков и снижению потребности в глюкозе. [27]
Как видно из данных табл. 57, показатель эффективности наиболее низкий ( 5, 21) в первой группе больных, где использовалось сочетанное введение промедола, димедрола и анальгина. Высокий показатель эффективности имеет введение дроперидола - 5 73, а налучшим показателем эффективности обладает схема VI, предусматривающая сочетанное введение дроперидола и оксибутирата натрия. [28]
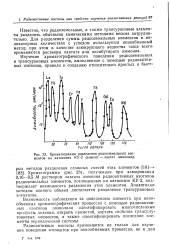 |
Хроматограмма разделения редкоземельных элементов на катионите КУ-2 ( элюент - лактат аммония. [29] |
Известно, что редкоземельные, а также трансурановые элементы разделить обычными химическими методами весьма затруднительно. Для разделения суммы редкоземельных элементов в индикаторных количествах с успехом используется ионообменный метод; при этом в качестве элюирующего вещества чаще всего применяются растворы лактата или оксибутирата аммония. [30]
Страницы: 1 2 3