Оксид
Cтраница 1
Оксид ХО3 имеет кислотный характер. Бариевые и свинцовые соли некоторых из этих кислот находят непосредственное практическое применение. Сильные окислительные свойства растворимых солей этих кислот в кислой среде широко используются в количественном анализе. Название элемента X связано с некоторым общим свойством его соединений. [1]
Оксид пристает к металлу. [2]
Оксиды s - металлов ПА группы образуются непосредственно с выделением большого количества тепла. [3]
 |
Теплоты образования ( - Д / / некоторых оксидов лантаноидов. [4] |
Оксиды / - металлов используют для получения специальных стекол и некоторых огнеупоров. [5]
 |
Некоторые свойства d - металлов III группы. [6] |
Оксиды этих металлов - прочные белые кристаллические тела, при их образовании выделяется большое количество энергии. [7]
 |
Соединения титана с кислородом и их широта области гомогенности. [8] |
Оксиды d - металлов IV группы образуются с большим выделением энергии и могут иметь различные степени окисления и формы химической связи. Для циркония и гафния более характерны соединения высшей степени окисления. [9]
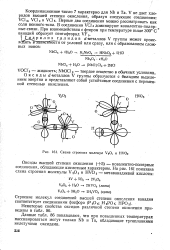 |
Схема строения молекул V2O3 и НУОз. [10] |
Оксиды d - металлов V группы образуются с большим выделением энергии и представляют собой устойчивые соединения с переменной степенью окисления. [11]
Оксиды d - металлов VII группы весьма многочисленны и образованы различными по своему характеру связями. Субоксиды для d - металлов VII группы уже не характерны. Возможные формы оксидов d - металлов VII группы приведены в табл. 97, причем малоустойчивые соединения взяты в скобки. [12]
Оксиды d - металлов семейства железа образуют гидраты основного характера, получающиеся в результате обменных реакций. [13]
Оксиды платиновых d - металлов можно получить непосредственным соединением с кислородом, но для большинства этих металлов они неустойчивы. Следует заметить, что свойства оксидов рутения и осмия подтверждают наличие ковалентных полярных связей в молекулах оксидов. [14]
Оксид, в котором золото проявляет степень окисления 1, может получаться только в процессе образования устойчивых комплексов ( см. стр. [15]
Страницы: 1 2 3 4