Оксид - молибден
Cтраница 1
 |
Внешний вид лопатки турбины первой ступени. [1] |
Оксиды молибдена МоО2 и Мо20б также возгоняются при 600 С и плавятся при 790 С. [2]
Оксид молибдена ( VI) возгоняется при сравнительно высокой температуре ( 750 С) и по мере продвижения электропечи легко конденсируется вблизи накаленной зоны на стенках контейнера. Полноту удержания молибдена в контейнере проверяют по постоянству массы гильзы. При наличии привеса более 15 мкг расчет содержания молибдена ведут по сумме привесов контейнера и гильзы. [3]
Оксид молибдена ( IV), или диоксид молибдена, MoOj образуется при при окислении молибдена водяным паром при 800 С, а также при восстановлении МоОз водородом или NHj при 470 С. [4]
Оксид молибдена ( VI) получают прокаливанием молибденовой кислоты или молибдата аммония при 500 - 600 С в фарфоровом тигле. [5]
Оксид молибдена ( VI) восстанавливают водородом в фарфоровой или стеклянной трубке ( рис. 1, 2) при 550 - 600 С до образования коричневого порошка. Водород предварительно следует пропустить через промывал-ку с водой. Для очистки продукта от возможной примеси оксида молибдена ( VI) его прогревают в той же трубке в токе хлороводорода при 200 - 300 С. Образующиеся оксихлориды отгоняются в холодную часть трубки. Оксид молибдена ( IV) на воздухе устойчив. [6]
Оксид молибдена ( У1) Мо03 и оксид вольфрама ( У1) WO3 проявляют кислотные свойства. [7]
Оксид молибдена ( VI) МоО3 - кристаллы светло-зеленого цвета, которые выше 600 С начинают возгоняться, поэтому при прокаливании этого соединения при высоких температурах наблюдаются потери молибдена. В водных растворах щелочей и аммиака МоО3 растворяется с образованием соответствующих молибдатов. Оксид молибдена ( VI) растворим также в минеральных кислотах. [8]
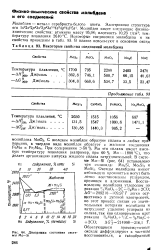 |
Некоторые свойства соединений молибдена. [9] |
Оксиды молибдена имеют небольшую прочность и могут быть легко восстановлены углеродом, кремнием и алюминием. [10]
Оксид молибдена ( IV), или диоксид молибдена, MoOi образуется при при окислении молибдена водяным паром при 800 С, а также при восстановлении МоОз водородом или NHs при f470 С. [11]
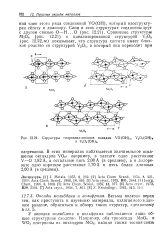 |
Структуры гидроксид-оксидов ванадия VO ( OH2, УзО4 ( ОН. [12] |
У оксидов молибдена и вольфрама наблюдается лишь общее структурное сходство. [13]
Сульфиды и оксиды молибдена и вольфрама с промоторами являются бифункциональными катализаторами ( с п - и р-проводимостями): они активны как в реакциях гидрирования-дегидрирования ( гемолитических), так и в гетеролитических реакциях гидрогенолиза гетеро-атомных углеводородов нефтяного сырья. Однако каталитическая активность Мо и W, обусловливаемая их дырочной проводимостью, недостаточна для разрыва углерод-углеродных связей. Поэтому для осуществления реакций крекинга углеводородов необходимо наличие кислотного компонента. [14]
Сульфиды и оксиды молибдена и вольфрама с промоторами являются бифункциональными катализаторами ( с п - и р - прово - дикостями): они активны как в реакциях гидрирования - дегидрирования ( гемолитических), так и в гетеролитических реакциях гидрогенолиза гетероатомных углеводородов нефтяного сырья. Однако каталитическая активность Мо и W, обусловливаемая их дырочной проводимостью, недостаточна для разрыва углерод - углэродных связей. Поэтому для осуществления реакций крекинга углэводородов необходимо наличие кислотного компонента. Следовательно, катализаторы процессов гидрокрекинга являются по существу минимум трифункциональными, а селективного гидрокрекинга - тетрафункциональными, если учесть их молекулярно - ситовые свойства. Кроме того, когда кислотный компонент в катализаторах гидрокрекинга представлен цеолитсодержащим алюмосиликатом, следует учесть также специфические крекирующие свойства составляющих кислотного компонента. Так, на алюмоси - ли ате - крупнопористом носителе - в основном проходят реакции первичного неглубокого крекинга высокомолекулярных углеводо - родов сырья, в то время как на цеолите - реакции последующего бо / ее глубокого крекинга - с изомеризацией среднемолекулярных углеводородов. [15]
Страницы: 1 2 3 4