Оксид - рений
Cтраница 2
Оксид технеция ( VII) Тс2О7 ( ДЯ2 8 - 11 17 кдж / моль) и оксид рения ( VII) Re207 ( ДЯяв8 - 1243 кдж / моль) - устойчивые кристаллические вещества желтого цвета. [16]
Некоторые оксиды гетероэлементов частично удерживают оксид рения ( VII) в контейнере, например оксиды фосфора и бора. Галогены поглощаются нагретым серебром вместе с оксидом рения. В таких сложных случаях возможен расчет состава полученной смеси в соответствии с соотношением атомов Re: El в анализируемом веществе. [17]
Электроосажденный рений также может быть разделительным слоем. Его применяют в производстве беспористой медной фольги; оксиды рения обладают электрической проводимостью и исключают образование пор в фольге. [18]
Для улучшения антифрикционных характеристик и предотвраще ния схватывания серебряных электрнческих контактов или подшипников скольжения применяют К. ЭП, содержащие в качестве второй фазы гра фит, дисучьфид молибдена, нитрид бора ичи оксиды рения. [19]
Для измерения очень высоких температур используют термопары из вольфрама и рения, вольфрама и графита, но их надо защищать от действия окислительной атмосферы, так как оксиды рения и вольфрама очень летучи, не говоря уже о графите. [20]
Навеску пробы 1 г растворяют в 2 мл воды. При анализе оксида рения ( VII), полученного из вольфрамовых отходов, к раствору добавляют Н2О2, раствор NH3 - H2O и 0 2 мл 10 % - ного раствора I SO. Затем добавляют 10 мл H2SO4 ( 1: 3) и раствор выпаривают до полного исчезновения белых паров. К остатку добавляют 2 мл H2SO4 ( 1: 1) и выпаривают досуха. На следующий день осадок серы отфильтровывают на плотный фильтр и промывают 10 раз 2 % - ным раствором гидроксиламинхлорида в l 6M HC1 и 5 раз водой. Осадок растворяют в смеси 1 мл H2SO4, 0 2 мл насыщенного раствора КС. Раствор слегка нагревают до растворения осадка, переводят в мерную колбу вместимостью 25 мл, доведя его объем до метки водой. Раствор анализируют методом ИВПТ с СРЭ. Градуировку проводят методом добавок. [21]
Оксид рения ( VII) сублимируется при 200 С. Конденсация Re2O7 в охлажденной гильзе затруднена образованием стойких туманов рениевой кислоты. Для поглощения оксида рения используют рулон из серебряной сетки или фольги длиной 40 мм и массой 1 г. Пер-ренат серебра нелетуч, негигроскопичен и хорошо сохраняет постоянство массы. [22]
Некоторые оксиды гетероэлементов частично удерживают оксид рения ( VII) в контейнере, например оксиды фосфора и бора. Галогены поглощаются нагретым серебром вместе с оксидом рения. В таких сложных случаях возможен расчет состава полученной смеси в соответствии с соотношением атомов Re: El в анализируемом веществе. [23]
С увеличением атомных масс повышается стабильность высоких степеней окисления переходных элементов. Это особенно заметно при сопоставлении свойств высших оксидов марганца, технеция и рения. Оксид марганца ( VII) при нагревании разлагается со взрывом и даже при 0 С неустойчив, соответствующий оксид технеция плавится без разложения при 119 5 С, а оксид рения ( VII) - столь прочное соединение, что его можно перегонять ( без разложения) при температурах выше 220 С. [24]
Предварительно 200мл этого раствора очищают от серы добавлением 2 мл 10 % - ного раствора К. Полученный осадок отделяют Центрифугированием. Раствор оксида рения или перрената аммония в пробирке нагревают до 80 С. Полученный осадок отделяют центрифугированием. Раствор с осадком хроматов центрифугируют. [25]
К ним в первую очередь относятся покрытия Ag-Re, нетускнеющие серебряные покрытия и любые другие покрытия, полученные за счет внедрения субмикрочастиц коллоидного размера, образующихся при определенных условиях в прикатодном пространстве или при введении дополнительных реагентов в чистые электролиты. Покрытие Ag-Re по своей структуре и составу является ультрамикрокомпозиционным, так как рений содержится в нем в виде основания ( оксид или гидроксид) известного ( ReO2) или неопределенного состава. При этом повышаются твердость и антифрикционные характеристики покрытия. КЭП серебро - оксид рения может быть с успехом использовано в деталях со скользящей поверхностью. [26]
Фосфорорганические соединения представлены в нашей практике как легкоокисляющимися на воздухе, так и трудно-сжигаемыми веществами. К первым относятся многие соединения фосфора ( III) - триалкенилфосфины, эфиры алкилфос-финистых кислот и др. Ко вторым - дифосфиноксиды, вещества, содержащие наряду с фосфором другие гетероэлементы. При наличии в веществе галогенов ( хлора, брома или иода) или серы можно определить четыре элемента в одной навеске, а в присутствии еще и ртути - пять. Из других летучих оксидов фосфорный ангидрид не задерживает OsO4, который может быть определен одновременно с галогеном и фосфором. Гетероэлементы, не образующие летучие оксиды, определяются вместе с P2Os по массе остатка расчетным путем. Оксид рения частично остается в контейнере вместе с оксидом фосфора. К ним относятся фосфорсодержащие карбораны, полициклоорганосилокеаны и другие полимеры, фосфиноборины, соединения с PF6 - rpyn - пами и др. Особенности анализа веществ, содержащих фосфор и марганец, описаны в разд. [27]
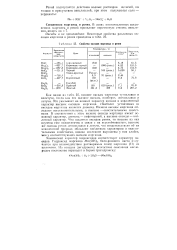 |
Свойства оксидов марганца и рения. [28] |
Как видно из табл. 25, низшие оксиды марганца тугоплавки и нелетучи, тогда как его высшие оксиды, наоборот, легкоплавки и летучи. Это указывает на ионный характер низших и ковалентный характер высших оксидов марганца. Наиболее устойчивым из оксидов марганца является диоксид. Низшие оксиды марганца обладают восстановительными, а высшие - окислительными свойствами. В соответствии с этим низшие оксиды марганца имеют основный характер, диоксид - амфотерный, а высшие оксиды - кислотный характер. Что касается оксидов рения, то низшие из них изучены еще недостаточно в связи с их неустойчивостью; высшие же оксиды рения легкоплавки и летучи, что свидетельствует об их ковалентной природе, обладают кислотным характером и окислительными свойствами, однако последние выражены у них слабее, чем у соответствующих оксидов марганца. [29]
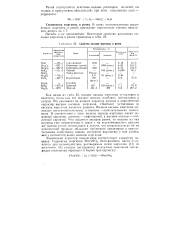 |
Свойства оксидов марганца и рения. [30] |
Страницы: 1 2 3