Низший оксид
Cтраница 1
Низшие оксиды обладают основными свойствами. [1]
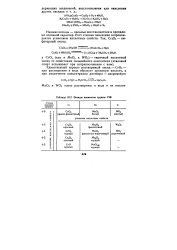
Низшие оксиды существуют почти у всех р -, d - и / - элементов. В табл. 20.5 приведены только те устойчивые и существующие при обычных условиях оксиды р-элементов, у которых степень окисления элементов на две единицы меньше, чем в высших оксидах: тах - 2, а также амфолиты и кислоты, образующиеся при взаимодействии данных оксидов с водой. [2]
Низшие оксиды и их соли являются восстановителями, а соединения высшей степени окисления - окислителями в окислительно-восстановительных реакциях. [3]
 |
Оксиды элементов группы VIB. [4] |
Низшие оксиды - сильные восстановители и проявляют основной характер. Рост степени окисления сопровождается усилением кислотных свойств. [5]
 |
Разрез кварцевой трубки для получения PrOj. [6] |
Низшие оксиды переводят в Рг6Оц кратковременным нагреванием до 00 С на воздухе. [7]
Низший оксид термически устойчив, проявляет слабые окислительные свойства и практически не проявляет восстановительных. Подобно PbO, Bi2O3 обладает практически только основными свойствами и нерастворим в щелочах. Большинство солей висмута малорастворимы. [8]
 |
Оксиды элементов группы VIВ. [9] |
Низшие оксиды - сильные восстановители и проявляют основной характер. Рост степени окисления сопровождается усилением кислотных свойств. [10]
Низшие оксиды углерода и кремния СО и SiO являются несолеобразующими оксидами, а оксиды двухвалентных германия, олова и свинца - GeO, SnO и РЬО - амфотерны-ми оксидами. [11]
Низшие оксиды углерода и кремния СО и SiO являются несолеобразующими оксидами, а оксиды двухвалентных германия, олова и свинца GeO, SnO и РЬО - амфотерными оксидами. [12]
 |
Типичные кристаллические решетки металлов. [13] |
Низшие оксиды данного металла имеют более основной характер, чем высшие. Это иллюстрируется данными для хрома. [14]
Гидроксид низшего оксида хрома обладает основными свойствами, высшего - кислотными. Запишем ряд: окись хрома СгО - гидроксид хрома ( II) Сг ( ОН) 2 - основание; полутораокись хрома - Сг ( ОН) 3, или НСг02 - амфотерное соединение; трехокись хрома ( хромовый ангидрид) Сг03 - хромовая Н2Сг04 и двухромовая Н2Сг207 кислоты. [15]
Страницы: 1 2 3 4