Низший оксид
Cтраница 3
Возможность изменения степеней окисления делает низшие оксиды и их соли восстановителями, а соединения высшей степени окисления - окислителями в окислительно-восстановительных реакциях. [31]
 |
Равновесные парциальные давления ( в МПа компонентов. [32] |
Заметнее хлорируются в отсутствие восстановителя низшие оксиды титана. По данным [28], заметная скорость хлорирования ТЮ наблюдается при 215 С, Ti2O3 - при 225 С, а ТЮ2 - только при температуре выше 800 С. В присутствии восстановителя диоксид титана хлорируется практически полностью. Соответственно приобретает отрицательное значение изменение изобарного потенциала реакции хлорирования диоксида титана в присутствии восстановителя. [33]
Определенная часть ТЮ2 восстанавливается до низших оксидов ( Ti203, TiO и др.), которые при обжиге изделий окисляются и могут также приводить к аномальному росту ( расширению) изделий. [34]
К соединениям кластерного типа относятся также низшие оксиды ниобия и тантала. [35]
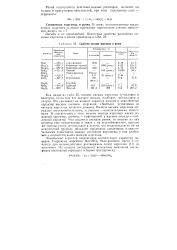 |
Свойства оксидов марганца и рения. [36] |
Как видно из табл. 25, низшие оксиды марганца тугоплавки и нелетучи, тогда как его высшие оксиды, наоборот, легкоплавки и летучи. Это указывает на ионный характер низших и ковалентный характер высших оксидов марганца. Наиболее устойчивым из оксидов марганца является диоксид. Низшие оксиды марганца обладают восстановительными, а высшие - окислительными свойствами. В соответствии с этим низшие оксиды марганца имеют основный характер, диоксид - амфотерный, а высшие оксиды - кислотный характер. Что касается оксидов рения, то низшие из них изучены еще недостаточно в связи с их неустойчивостью; высшие же оксиды рения легкоплавки и летучи, что свидетельствует об их ковалентной природе, обладают кислотным характером и окислительными свойствами, однако последние выражены у них слабее, чем у соответствующих оксидов марганца. [37]
К соединениям кластерного типа относятся также низшие оксиды ниобия и тантала. [38]
Согласно [5], ТЬО2 получают взаимодействием низших оксидов с 0 1 и. [39]
Формирование монослоя хемосорбированного кислорода, соответствующего низшему оксиду РЮ, заканчивается при потенциале 1 4 - 1 5 В. [40]
Формирование монослоя хемосорбировашого кислорода, соответствующего низшему оксиду РЮ, заканчивается при потенциале 1 4 - 1 5 В. [41]
Кроме того, для титана известны и низшие оксиды Ti2O3 и ТЮ. [42]
Кроме того, для титана известны и низшие оксиды Т120з и ТЮ. [43]
Продажный препарат почти всегда содер жит примеси низших оксидов, преимущественно Р О6, а иногда и белый фос фор. [44]
Если металл образует оксиды разной валентности, то низшие оксиды хлорируются при меньшей температуре и с большей скоростью. [45]
Страницы: 1 2 3 4