Летучий оксид
Cтраница 3
 |
Рост оксидной пленки на железе Наилучшие по стойкое. [31] |
Практически вообще не пассивируются при высоких температурах d - металлы, обладающие высокими степенями окисления и, следовательно, летучими оксидами: Mo, W; Mb; Та; Re. Температура кипения их оксидов ниже температуры плавления соответствующих металлов и поэтому оксиды улетают в газовую фазу, обнажая поверхность металла для дальнейшего окисления. [32]
При обжиге сульфидов и других бинарных соединений наименее активных металлов ( ртуть, серебро, платина и золото) неметаллы дают летучие оксиды, а металлы восстанавливаются. Такие процессы сопровождаются ростом энтропии и оказываются термодинамически выгодными при невысоких температурах. [33]
Некоторые металлы ( Mo, W, Nb, Та, Re), окисляясь при высоких температурах на воздухе, образуют летучие оксиды. Последние кипят ниже, чем плавятся соответствующие им металлы, следовательно не образуют на поверхности таких металлов защитных пленок. Эги металлы называют нежаростойкими. [34]
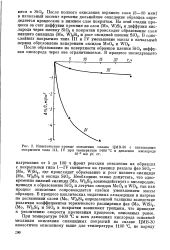 |
Кинетические кривые окисления сплава ЦМВ-30 с силицидным покрытием типа III, IV при температуре 1400 С и давлении кислорода. [35] |
Необходимо также допустить, что одновременно низший силицид ( Mo, W) 5Si3 взаимодействует с кислородом, приводя к образованию Si02 и летучих оксидов Мо03 и W03, так как процесс окисления сопровождается слабым уменьшением массы образцов. В процессе циклических медленных охлаждения и нагрева по достижении слоем ( Mo, W) 5Si3 определенной толщины вследствие различия коэффициентов термического расширения фаз ( Mo, W) Si2, ( Mo, W) 6Sis и Si02 в покрытии возникают трещины, что приводит к увеличению скорости протекания процессов, описанных ранее. [36]
Паравольфрамат аммония, ( NH O 12WOs 5НОН, начинает разлагаться при сравнительно низкой температуре: 180 - т - 200 С, что сопровождается получением летучих оксидов вольфрама. [37]
Иногда их можно удалить с помощью нагревания образца на месте ( т.е. внутри СВВ-камеры), в результате чего эти примеси могут десорбировать в вакуум в виде летучих оксидов, сульфидов или карбидов или могут растворяться внутри твердого тела. В результате на поверхности остается очень малый уровень загрязнения. Чтобы достичь значительных скоростей удаления этих примесей, могут понадобиться температуры, близкие к точке плавления материала образца. [38]
 |
Установка для отгонки и поглощения аммиака. [39] |
Попытки ускорить стадию окисления в методе Кьельдаля введением сильных окислителей, таких, как хлорная кислота, пер-манганат калия и перекись водорода, оказались неудачными, поскольку ион аммония частично окисляется до летучих оксидов азота. [40]
При кипячении водных растворов теряются борная и азотная кислоты, галогеноводородные кислоты; фосфорная кислота отгоняется из горячих концентрированных растворов серной и хлорной кислот. Летучие оксиды могут быть потеряны из горячих кислых растворов; к ним относятся тетраоксиды осмия и рутения, а также гептаоксид рения. [41]
Для этого в реактор вводят кислород или летучие оксиды, например As2O3 при получении арсенидов. Иногда летучие оксиды создают ( генерируют), помещая в реактор смесь металлического компонента со своим высшим оксидом, взятых в стехиометрическом соотношении. [42]
Оксиды примесей всплывают на поверхность и образуют шлак. Отдельные летучие оксиды могут переходить частично и в парообразное состояние. Таким путем удается удалить основную часть примесей: Al, Pb, Mn, Zn, Sn, Fe, Ni, S и частично Sb, As, Bi; не окисляются и остаются в меди золото, серебро, а также селен и теллур. [43]
Из тяжелых платиновых металлов наиб, химически активен, в мелкораздробленном состоянии окисляется кислородом воздуха при комнатной темп-ре. Летучий оксид OsOt токсичен, обладает неприятным запахом. [44]
Концентрат вначале подвергают окислит, обжигу при 5 50 - 600 С в многоподовых печах или в печах с кипящим слоем. Если в концентрате содержится Ке, при обжиге образуется летучий оксид Ке2О7, к-рый удаляют вместе с печными газами. Чистый МоО3, необходимый для произ-ва металлич. [45]
Страницы: 1 2 3 4