Оксисульфид
Cтраница 2
Сульфид и оксисульфид таллия применяют для изготовления фотоэлементов, обладающих высокой чувствительностью к действию инфракрасных лучей. Эти фотоэлементы используют для сигнализации в темноте или густом тумане. Таллофидные фотоэлементы особенно важны в авиации. Их применяют для изготовления инфракрасных прожекторов, указывающих место посадки на затемненном аэродроме, а также используют в инфракрасной фотографии. [16]
Сульфид и оксисульфид таллия используют для изготовления фотоэлементов, чувствительных к воздействию инфракрасного излучения и широко применяемых в авиации. [17]
Сначала образуется оксисульфид нептуния NpOS, который после длительной обработки превращается в полуторный сульфид. [18]
Для получения оксисульфида иттербия смесь Yb2O3 с 5 % - ным избытком Yb2S3 нагревают до 1350 С в среде аргона [ 198, с. Оксисульфид иттербия трудно растворим в концентрированной соляной кислоте, легко растворяется в царской водке. [19]
В сталях имеются оксисульфиды с переменным содержанием церия и лантана, которые имеют глобулярную форму. [20]
Сначала появляется промежуточный оксисульфид NpOS, который после длительной обработки превращается в полуторный сульфид. Фрид и Дэвидсон [19] отметили, что система нептуний - сера по своим свойствам занимает промежуточное положение между системами уран - сера и плутоний - сера. [21]
Образование и поведение оксисульфидов могут иметь поэтому большое значение для первой из двух реакций. Должна быть изучена термодинамика образования оксисульфидов и их стабильность при высоких концентрациях сероводорода. Подобным образом должно быть изучено соотношение между увеличивающейся стойкостью к сульфидированию и изменениями активности катализаторов гидронитроочистки и гидросероочистки. [22]
При взаимодействии этих оксисульфидов с 5 % - ным раствором НС1 они полностью растворяются, при этом половина серы выделяется в форме H2S, а вторая - в виде элементарной серы. Моносульфиды празеодима и неодима легко реагируют с разбавленными кислотами, причем при реакции с НС1 и СН3СООН выделяются H2S и Н2 ( 2: 1 по объему), при растворении в НМО3 и в концентрированной H2SO4 выпадает сера. Перекись водорода окисляет PrS и NdS: при нагревании на воздухе медленное окисление этих сульфидов начинается при 200 С. С, а при 600 С переходят в основные сульфаты состава ( МЮ) 25О4 - Рг2О25 и Nd. Они растворяются в разбавленных неорганических кислотах, хотя и медленнее, чем соответствующие сульфиды. Кроме того, эти Оксисульфиды растворяются на холоду в разбавленной уксусной кислоте. Растворами иода и перманганата Pr2O2S и Nd2O2S не окисляются. [23]
В [112] был синтезирован оксисульфид кадмия с концентрацией окиси кадмия от 0 01 до 5 мол. [24]
Сульфид цирконила ( или оксисульфид циркония), ZrOS, представляет собой желтый порошок с плотностью 4 87 г / см3, воспламеняющийся при нагревании. [25]
В нормальных условиях сульфиды и оксисульфиды, как правило, устойчивы в сухом воздухе, а во влажном некоторые из сульфидов медленно гидролизуются, выделяя сероводород. При 200 - 300 на воздухе начинается их окисление с образованием основных сульфидов и окислов. Высшие сульфиды термически неустойчивы и при сравнительно низкой температуре разлагаются, выделяя серу. Сульфиды не растворяются в воде. [26]
При нормальных условиях сульфиды и оксисульфиды, как правило, устойчивы в сухом воздухе, а во влажном некоторые из сульфидов медленно гидролйзуют-ся с выделением сероводорода - При 200 - 300 на воздухе начинается их окисление с образованием основных сульфатов и окислов. Высшие сульфиды термически неустойчивы и при сравнительно низких температурах разлагаются с выделением серы. [27]
Для соблюдения равновесия оксид - оксисульфид из уравнений (8.7) и (8.8) константа К должна составлять 106 / 103 101, т.е. содержание серы в металле должно превышать содержание кислорода в 10 раз. Аналогично для равновесия сульфид - оксисульфид из уравнений (8.9) и (8.10) константа К [ S ] 2 / [0] 2 Ю8 / 106 102, т.е. содержание серы должно превышать содержание кислорода в 100 раз. [28]
В нормальных условиях сульфиды и оксисульфиды, как правило, устойчивы в сухом воздухе, а во влажном некоторые из сульфидов медленно гидролизуются, выделяя сероводород. При 200 - 300 на воздухе начинается их окисление с образованием основных сульфидов и окислов. Высшие сульфиды термически неустойчивы и при сравнительно низкой температуре разлагаются, выделяя серу. Сульфиды не растворяются в воде. [29]
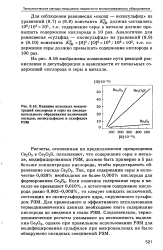 |
Влияние исходных концентраций кислорода и серы на последовательность образования включений оксидов, оксисульфидов и сульфидов РЗМ. [30] |
Страницы: 1 2 3 4