Оксихинона
Cтраница 1
Оксихиноны редко встречаются в виде гликозидов и поэтому легко экстрагируются органическими растворителями. Морских ежей сначала обрабатывают кислотой для удаления неорганических материалов из их раковин. Для проявления хроматограмм используют неполярные растворители или их смеси. [1]
Оксихиноны дают интенсивно окрашенные щелочные соли; хиноны всех типов образуют ярко окрашенные оюсониевые соли в концентрированной серной кислоте. Хинонное кольцо содержит только две двойные связи и является неароматическим; хиноны представляют собой аналоги а р-ненасыщенных кетонов с открытой цепью, но обладают значительно большей реакционной способностью. [2]
Оксихиноны дают интенсивно окрашенные щелочные соли; хиноны всех типов образуют ярко окрашенные оксониевые соли в концентрированной серной кислоте. При действии мягких восстановителей они превращаются в бесцветные гидрохиноны. [3]
Мы имели в своем распоряжении оксихиноны бензольного, нафталинового, антраценового и нафтаценового рядов; в этом сообщении мы хотим изложить данные, полученные для производных бензохинона. Из этих соединений хлораниловую кислоту или 3 6-дихлор - 2 5-диокспбензохинон - 1 4 уже используют как аналитический реагент. [4]
Йрко выраженной способностью образовывать соединения с металлами обладают оксихиноны. Природные вещества, содержащие оксихиноны, - ализарин и кошениль - веками применялись для окраски текстиля, и было известно, что в этом процессе участвуют металлы. К образованию комплексов с металлами способны простые оксибензохиноны, и особенно бксинафтохиноны и оксиантра-хиноны. Выше приводится ряд оксихинонов, применяющихся в качестве индикаторов при комплексонометричееких титрованиях. [5]
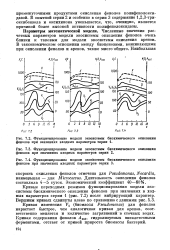
В опытной серии 2 и особенно в серии 3 содержание 1 2 3-три-оксибензола и оксихинона уменьшается, что, очевидно, является причиной более высокой активности полифенолоксидазы. [7]
Кипячение в водном растворе едкого натра и обработка алкоголятами в диметилформамиде или диметилсульфоксиде приводит непосредственно к оксихинону CXVIII и алкоксипроизводным CXIX. В случае вступления электроноакцепторной CN-группы, повышающей окислительно-восстановительный потенциал хинона, конечным продуктом является 4-циангидрохинон CXXI, для перевода которого в СХХ нужна обработка сильным окислителем. [8]
Реакция Тиле ( 1898), при которой в присутствии катализаторов серной кислоты или эфирата трехфтористого бора хинону присоединяется уксусный ангидрид с образованием триацетата триоксинафта-лина, дает возможность получать оксихиноны. [9]
Реакция Тиле ( 1898), при которой в присутствии катализаторов серной кислоты или эфирата трехфтористого бора к хинону присоединяется уксусный ангидрид с образованием триацетата триоксинафта-лина, дает возможность получать оксихиноны. [10]
Йрко выраженной способностью образовывать соединения с металлами обладают оксихиноны. Природные вещества, содержащие оксихиноны, - ализарин и кошениль - веками применялись для окраски текстиля, и было известно, что в этом процессе участвуют металлы. К образованию комплексов с металлами способны простые оксибензохиноны, и особенно бксинафтохиноны и оксиантра-хиноны. Выше приводится ряд оксихинонов, применяющихся в качестве индикаторов при комплексонометричееких титрованиях. [11]
Соединения с пиридиновым ( CXXVIII) и пиразиновым ( CXXIX) атомами азота обладают наиболее прочной водородной связью. По величине AvoH и Д6Он ( см. табл. 3) они превосходят оксихиноны, что подтверждает мнение180 о большей прочности связей О - Н N по сравнению со связями О - Н - - - О. [12]
Получение оксихинока из оксигидрохинока. После упаривания и охлаждения темно-желтого эфирного раствора выпадает 1 - 2 г оксихинона в виде сростков желтых призм. Для очищения продукт растворяют в хлороформе, осаждают петролейным эфиром и затем перекристаллизовывают из бензола. Полученный таким образом оксихинон представляет собою прекрасные, резкоочерченные прямоугольные пластинки, легкорастворимые в воде, алкоголе, ацетоне. Водный раствор желтого цвета быстро бурсе i; спиртовый раствор коричневого цвета. Эфирные растворы оксихинона прочны. Кристаллическое вещество хранится в темноте без изменения и течение нескольких дней, а затем темнеет и осмо-ляется. Продукт не имеет запаха, но вызывает чихание; при нагревании не плавится, но при 120 темнеет, а при 124 становится черным. [13]
Соединения с пиридиновым ( CXXVIII) и пиразиновым ( CXXIX) атомами азота обладают наиболее прочной водородной связью. По величине AvOH и Аб0н ( см. табл. 3) они превосходят оксихиноны, что подтверждает мнение180 о большей прочности связей О - Н - - N по сравнению со связями О - Н - - - О. [14]
Фенолы, растворенные в сточных водах, относительно легко окисляются кислородом воздуха. При взаимодействии с кислородом фенолы претерпевают глубокие структурные превращения: гидроксилируются, образуют хиноны, оксихиноны, карбоновые, гу-миновые кислоты, перекисные соединения, а также продукты уплотнения. Дальнейшее окисление может привести к образованию диоксида углерода и воды. Глубина превращения фенолов зависит от параметров окисления. Например, степень разложения метилрезорциновой и диметилрезорциновой фракций [368] при температуре сточной воды 40 С и рН 9 5 - 13 0 составляет 30 - 50 %, причем наблюдается образование продуктов уплотнения и конденсации фенолов, плохо растворимых в воде. [15]
Страницы: 1 2