Оксо-группа
Cтраница 1
Оксо-группы всех исследованных нами соединений не мешают списанной ориентации реагентов в переходном состоянии, тогда как влияние атомов хлора при двойных связях следует учитывать, хотя оно, по всей вероятности, невелико. Что касается атомов хлора циклических дихлорметиленовых групп в соединениях I, II. [1]
Оксо-группа в группировке RCO -, в которой R: ( а) алифатический ( Р) циклический ( и) Карбокси-группа н циано-группа. Гетероциклические группы, присоединенные атомом углерода. [2]
Кетогрушш сложных соединений называют также оксо-группами. Эти группы шумеруются подобно другим заместителям. [3]
При взаимодействии TiG4 с Н3О образуются соединения, содержащие гидроксо - и оксо-группы. [4]
При взаимодействии TiCl4 с Н2О образуются соединения, содержащие гидроксо - и оксо-группы. [5]
В кетонах карбонильная группа связана с двумя углеводородными радикалами и называется также квтогруппой или оксо-группой. [6]
Качественно аналогичен дитизону реагент дифенилкарбазон, который отличается только тем, что вместо тио-группы имеет оксо-группу. Кислород обладает меньшей, чем сера, комплексо-образующей способностью по отношению к катионам с заполненными d - уровнями, поэтому весьма вероятно, что в фиолетово-синем внутрикомплексном соединении этого реагента с ионом Hg ( II), образующемся в нейтральных или умеренно щелочных растворах, центральный атом связан с атомами азота. Это, по-видимому, справедливо также и в отношении окрашенных соединений, образуемых дифенилкарбазидом ( дигидропроизводным дифенилкарбазона) с такими металлами, как кадмий, кобальт, медь, свинец, ртуть, никель, серебро и цинк. Введение в молекулу дифенилкарбазида двухп, п - нитрогрупп понижает его растворимость в воде, вследствие чего ионы кадмия и других металлов образуют нерастворимые осадки. [7]
Дигидроксипиразины подобно 4 6-дигидроксипиримиди-нам не существуют в бис-амидной форме, и как только одна из гидроксильных групп таутомеризуется в оксо-группу ( 134) и ( 135), вся структура стабилизуется в силу сопряжения группировок имидокислоты. [8]
Дигидроксипиразины подобно 4 6-дигидроксмниримидн-нам не существуют в опс-амндной форме, и как только одна из гидроксильных групп таутомеризуется в оксо-группу ( 134) и ( 135), вся структура стабилизуется в силу сопряжения группировок имидокнслоты. [9]
При смешивании растворов V2 и VO2 получается V3, но в качестве промежуточного соединения образуется коричневое вещество, в котором имеется мостиковая оксо-группа VOV4 [14], оно напоминает соединение хрома ( Ш) СгОСг4, образующееся при окислении Сг2 в условиях, когда можно ожидать образования комплекса Cr [ V, а именно при окислении ионами Т13, отнимающими два электрона. [10]
По-видимому, декарбокеилирование происходит с промежуточным образованием шестичленного переходного состояния, чему способствует возникновение водородной связи между атомом водорода гидроксильной группы и атомом кислорода оксо-группы. [11]
По-видимому, декарбокснлироьанне происходит с промежуточным образованием шестичленного переходного состояния, чему способствует возникновение водородной связи между атомом водорода гидроксильной группы н атомом кислорода оксо-группы. [12]
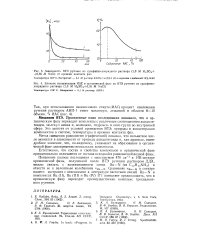 |
Влияние концентрации НАС в органической фазе на ВТЭ рутения из сульфатно-хлоридного раствора ( 1 0 М H2SO4 0 35 M NaCl Температура 100 С. Экстрагент - 0 1 М раствор АНП-1. [13] |
Проведенные нами исследования показали, что в органическую фазу переходят комплексы с различным соотношением ацидоли-гандов, молекул амина и, возможно, гидроксо - и оксо-групп во внутренней сфере. Это зависит от условий проведения ВТЭ, природы и концентрации компонентов в системе, температуры и времени контакта фаз. [14]
Такая конденсация с участием карбонильной группы и ароматического ядра, протекающая под влиянием кислотных агентов ( в частном случае прототропно), лежит в основе многих конденсаций, приводящих к образованию карбо - и гетероциклических структур, например, нагревание фенилового эфира ацетоуксусной кислоты с серной кислотой приводит к синтезу кумарина. Аналогичный процесс а таки карбокатиона, образовавшегося при протонировании оксо-группы, лежит в основе синтеза хинолинов по Дебнер-Миллеру или изохинолинов по Померанцу-Фричу. [15]
Страницы: 1 2