Оксо-реакция
Cтраница 2
Использование координации для активации малых молекул наиболее ярко прослеживается на примере оксо-реакций и сходных процессов введения окиси углерода и водорода в подходящие органические соединения. Реакция катализируется солями кобальта, которые участвуют в ней в виде НСо ( СО) 4 и Co2 ( CO) g, а реакционная смесь состоит из ненасыщенного углеводорода или спирта, окиси углерода и водорода, находящихся под давлением, и какой-либо соли кобальта. [16]
Все эти соединения образуют в условиях гидроформилирования карбонилы кобальта - собственно катализатор оксо-реакции. [17]
Неоднократно сообщалось, что олефины с внутренним и конечным положением двойной связи в оксо-реакции всегда дают продукты с одним и тем же соотношением изомерных альдегидов. [18]
Хотя каждое из этих исследований неполно и включает много допущений, из общего рассмотрения можно предложить разумный механизм оксо-реакции. Важной особенностью такой реакции является то, что должны образоваться координационно-ненасыщенные или сольватированные формы, чтобы координировать ненасыщенные органические субстраты. Тогда реакция протекает как серия таких координации, сопровождаемых реакциями внедрения, которые фактически являются реакциями миграции лиганда. [19]
В условиях технического оксосинтеза ( высокая температура, высокое давление, малая концентрация катализатора) имеет место реакция с водородом, так как, во-первых, концентрация гидрокар-бонила во время реакции крайне незначительнаат, и, во-вторых, как указывали Нива и Ямагучи44, скорость реакции, выраженной уравнением ( 6), меньше скорости оксо-реакции. К концу реакции, когда уже ве ь исходный олефин прореагировал и имеются только конечный продукт и ацил-кобальткарбонил, можно ожидать, что восстанавливающим агентом будет гидрокарбонил, так как он больше не захватывается исходным олефином и может взаимодействовать с ацилкобальто-вым соединением. [20]
В условиях технического оксосинтеза ( высокая температура, высокое давление, малая концентрация катализатора) имеет место реакция с водородом, так как, во-первых, концентрация гидрокар-бонила во время реакции крайне незначительна37, и, во-вторых, как указывали Нива и Ямагучи44, скорость реакции, выраженной уравнением ( 6), меньше скорости оксо-реакции. К концу реакции, когда уже весь исходный олефин прореагировал и имеются только конечный продукт и ацил-кобальткарбонил, можно ожидать, что восстанавливающим агентом будет гидрокарбонил, так как он больше не захватывается исходным олефином и может взаимодействовать с ацилкобальто-вым соединением. [21]
В общем можно сказать, что оксо-реакция подчиняется законам гидрирования: легко гидрирующиеся этиленовые связи также легко присоединяют и альдегидную группу. Оксо-реакции свойственна в исходном олефине миграция кратной связи в а-положение. [22]
Технология оксо-реакции, получение альдегидов и спиртов. [23]
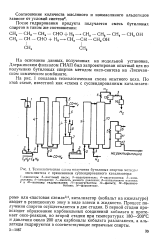 |
Технологическая схема получения бутиловых спиртов методом оксо-синте. а с применением суспендированного катализатора. [24] |
Процесс получения спиртов осуществляется в две стадии. В первой стадии происходит образование карбонильных соединений кобальта и протекает оксо-реакция, во второй стадии при температурах 180 - 200 С и давлении около 200 атм карбонилы кобальта разлагаются, а альдегиды гидрируются в соответствующие первичные спирты. [25]
Дигидронафталин не присоединяет альдегидной группы. Стирол характеризуется пониженной реакционной способностью; кроме того, в условиях оксо-реакции он полимеризуется и лишь в наиболее благоприятных случаях дает ( и то не более 10 - 20 %) фонилпропанол. [26]
Из приведенных выше соображений очевидно, что в качестве катализатора оксосинтеза можно применять кобальт в практически любой форме, поскольку при обычных условиях происходит, превращение его в дикобальтоктакарбонил. Этот вывод в равной степени относится к органическим солям кобальта, например солям октановой или нафтеновых кислот. Торговые сорта этих солей ( выпускаемых в продажу в качестве сиккативов для высыхающих масел) вполне пригодны для использования при оксо-реакции. [27]
Эта реакция идет при 120 - 150 и давлении 200 атм в присутствии йодистого никеля. Промышленное использование данной реакции тормозится сильным корродирующим действием Н J, что делает необходимым дорогостоящее платинирование или тантализирование аппаратуры. Таковы возможности реакции оксосинтеза, представляющие широкий интерес для производства синтетических высококачественных смазочных масел и других продуктов органического синтеза. Оксо-реакция дает возможность более рационально, в комплексном плане, проводить на основе водяного газа также и производство моторных топлив. [28]
В процессе неизбежно образуется некоторое количество воды; общее ее количество составляет - 1 вес. Следует отметить, что образования парафинов за счет насыщения олефинового сырья почти не происходит. По-видимому, это обусловлено гетерогенным катализом, где кобальт применяют в твердом состоянии. Между тем оксо-реакция является типичной гомогенной каталитической реакцией. [29]
Страницы: 1 2