Олдридж
Cтраница 2
В 1954 г. Ю. Ю. Лурье и В. А. Пановой [8] был разработан более чувствительный и быстрый метод определения цианидов, основанный на реакции, предложенной Олдриджем. [16]
Олдридж [22] описывают применение естественных способов очистки промышленных стоков трех больших заводов ( компании Дюпон в США), сбрасывающих стоки в крупные водоемы с большой самоочистительной способностью. [17]
Другим представителем амидофосфатов является димефокс [ ( CH3) 2N ] 2P ( O) F. Олдридж и Бернес [7] показали, что срезы печени превращают его в мощный антихолинэстеразный яд. Фенуик и др. [37] исследовали этот эффект более подробно. Печень самцов крыс оказалась приблизительно в 4 раза эффективнее, чем печень самок, что в известной мере напоминало действие печени на шрадан. Однако из трех изученных видов животных печень крысы оказалась наименее эффективной, а печень кролика - наиболее эффективной; в случае шрадана отношения были обратными. [18]
К сожалению, нет полной уверенности в том, что фермент сыворотки крыс, который гидролизует фенилбензоат и триацетин, является А-эстеразой. Олдридж [ 3, 4 6 тщательно исследовал невероятно сложную систему эстераз сыворотки, но он не использовал ни фе-нилбензоата, ни триацетина в качестве субстратов для сывороточных ферментов крыс. Был испытан трибутирин, но он гидролизо-вался очень плохо. В панкреатической железе ив мозге крыс гидролиз триацетина осуществляется главным образом ферментом В-типа ( он не тормозился параоксоном и не гидролизовал его) и лишь на 15 % А-эстеразой. Если в сыворотке существует такое же распределение, то приведенные выше результаты следует отнести за счет частичной способности гидролизовать параоксон и ТЭПФ. [19]
Олдридж [22] описывают применение естественных способов очистки промышленных стоков трех больших заводов ( компании Дюпон в США), сбрасывающих стоки в крупные водоемы с большой самоочистительной способностью. [20]
Наличие мощных водоемов не исключает осложнений при сбрасывании в них сточных вод. Так, по В. Олдриджу [22], для завода Олд Гихсцрн в США трудности вызывает сбрасывание стоков из водохранилища в реку и тщательное смешение их. При отсутствии ветра стоки в реке размещаются в определенных слоях и не смешиваются с ее водами. Поэтому рекомендуется отводить эти стоки в участки. [21]
Наличие мощных водоемов не исключает осложнений при сбрасывании в них сточных вод. Так, по В. Олдриджу [22], для завода Олд Гихорн в США трудности вызывает сбрасывание стоков из водохранилища в реку и тщательное смешение их. Установлено, что при увеличении плотности воды на 0 0006 происходит образование слоев воды различной плотности. При отсутствии ветра стоки в реке размещаются в определенных слоях и не смешиваются с ее водами. Поэтому рекомендуется отводить эти стоки в участки. [22]
Тем не менее реакция с водой происходит одновременно, а в особых случаях может стать преобладающей. Так, Олдридж и Дэвисон [49] нашли, что во время ингибирования тетраэтилпирофосфатом холинэсте-разы, связанной с поверхностью эритроцитов, гидролизу подвергается гораздо большая часть ангидрида, чем в действительности связывается ферментом. [23]
Выбор схем II-VI был обусловлен следующими обстоятельствами. В работах Олдриджа и О Брайна высказано предположение, что на определенной стадии ингибирования фермента возможна реактивация. [24]
Но даже если отбросить эти примеры ошибочных названий, то все равно приходится констатировать, что и в наименовании тех ферментов, индивидуальность которых установлена, нет единообразия. Дополнительная классификация была введена Олдриджем [ 31, который предложил применять термин А-эстеразы для эстераз, которые не угнетаются под действием ФОС, а термин Б - эстеразы к тем, для которых ФОС являются ингибиторами. [25]
В качестве доказательства, свидетельствующего о том, что торможение холинэстеразы ФОС представляет собой процесс фосфо-рилирования, выше уже указывалось, что скорость спонтанной реактивации зависит только от диалкильной части молекулы ФОС, ( см. стр. Для холинэстеразы эритроцитов кролика, по данным Олдриджа [ б ], скорость реактивации убывает в ряду: метил ] этил изопропил. Однако, как показал Дейвисон [34] на нескольких образцах ложной холинэстеразы крысы, диэтилфосфорилированный фермент реактивируется с большой скоростью ( период полувосстановления при рН 7 8 и 37 составлял 5 час); в этих же условиях ни диметил -, ни диизопропилфосфорил - фермент не восстанавливали своей активности наполовину даже за 200 час. Хоббигер [56] показал, что диэтилфосфорилированная холинэстераза сыворотки человека вообще не реактивируется спонтанно. [26]
Акционерное предприятие Лессинг, специализирующееся на изготовлении зубных щеток, выплатило в конце года держателям акций дивиденд в сумме 210 франков на каждую акцию. Олдридж прогнозирует постоянный рост дивидендов на ближайшие 5 лет по норме 7 % в год. [27]
Гардинер и Кильби3 показали с помощью меченого октаметила, что для угнетения холинэстеразы внутри организма требуется в 79J - 5000 раз меньше препарата, чем для той же степени угнетения холинэстеразы при опытах вне организма. Это привело к выводу, что октаметил превращается в организме животных в какие-то новые, во много раз более активные соединения. Олдридж и Барнес5 испытали в подобных опытах еще несколько соединений и нашли, что тиофос в организме животных активируется примерно в 10 раз, метафос в 12 раз. По нашим данным, в опытах с кроликами найдено, что при сравнении по дозам, вызывающим 50 % угнетения холинэстеразы, метафос активируется в 24 - 25 раз, а при сравнении по дозам, вызывающим 80 / о угнетения-от 73 до 260 раз. [28]
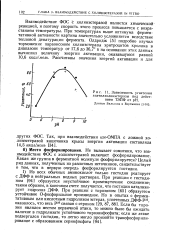 |
Зависимость угнетения ацетилхолинэстеразы под действием ТЭПФ от рН. [29] |
Взаимодействие ФОС с холинэстеразой является химической реакцией, и поэтому скорость этого процесса повышается с возрастанием температуры. При температурах выше оптимума ферментативной активности картина значительно усложняется вследствие тепловой денатурации фермента. Олдридж [ 51 подробно изучил торможение параоксоном холинэстеразы эритроцитов кролика в диапазоне температур от 17 6 до 36 7 и на основании этих данных вычислил величину энергии активации, оказавшуюся равной 10 6 ккал / моль. [30]
Страницы: 1 2 3