Зависимость - константа - диссоциация
Cтраница 1
Зависимость констант диссоциации от температуры часто бывает немонотонной. Во многих случаях с ростом температуры константы диссоциации сначала возрастают, а затем уменьшаются. Тепловой эффект диссоциации кислот неодинаков, поэтому изменение констант диссоциации с температурой у разных кислот имеет разный характер и сила кислот, характеризуемая величиной рК, с температурой изменяется неодинаково. Нередко одна кислота более сильная, чем другая при 25 С, становится менее сильной, например, при 70 С. [1]
Установленные предварительные зависимости констант диссоциации гидроксильных групп от характера водородной связи, образующейся в азокрасителях, свидетельствуют о наличии закономерностей, позволяющих по величине рК судить об образовании или прочности водородных связей. [2]
По зависимости константы диссоциации от температуры рассчитывают для растворов слабых электролитов ряд термодинамических функций. [3]
Для электролитов средней силы зависимость константы диссоциации, определенной по методу Оствальда, от концентрации оказывается существенно более сильной, чем для слабого электролита. Причина заключается в том, что при тех же концентрациях электролита достигается более высокая концентрация ионов. [4]
Почти все точные данные о зависимости констант диссоциации от температуры были получены путем измерения электродвижущих сил элементов без жидкостных соединений, содержащих слабые электролиты. Кроме того, все имеющиеся в настоящее время точные значения констант диссоциации для растворов в смесях воды с неводными растворителями в широком интервале температур были получены также путем измерения электродвижущих сил элементов без жидкостных соединений. В настоящей главе будут рассмотрены основы этого метода и его применение к определению констант диссоциации воды, слабых кислот и - амфолитов в воде и в водных растворах солей, а также в смесях воды с органическими растворителями. Будут описаны методы определения зависимости констант диссоциации от температуры и рассмотрены таблицы термодинамических величин, связанных с реакциями диссоциации. [5]
Почти все точные данные о зависимости констант диссоциации от температуры были получены путем измерения электродвижущих сил элементов без жидкостных соединений, содержащих слабые электролиты. Кроме того, все имеющиеся в настоящее время точные значения констант диссоциации для растворов в смесях воды с неводиыми растворителями в широком интервале температур были получены также путем измерения электродвижущих сил элементов без жидкостных соединений. Будут описаны методы определения зависимости констант диссоциации от температуры и рассмотрены таблицы термодинамических величин, связанных с реакциями диссоциации. [6]
Гальбан и Эберт [222], изучая зависимость классической константы диссоциации от концентрации электролитов в растворе, попытались определить значение истинной константы диссоциации, но избрали неудачный способ экстраполяции, приняв за абсциссу корень кубичный из общей ионной концентрации. [7]
Более поздние исследования, посвященные изучению зависимости констант диссоциации от среды и температуры, показали, что необходима большая осторожность при попытках создать теорию, устанавливающую зависимость констант диссоциации от строения слабых электролитов. [8]
Более поздние исследования, посвященные изучению зависимости констант диссоциации от среды и температуры, показали, что необходима большая осторожность при попытках создать теорию, устанавливающую зависимость констант диссоциации от строения слабых электролитов. [9]
Гэрни [ 66а ] выдвинул теорию для объяснения зависимости констант диссоциации от температуры, причем Боген [666] придал этой теории форму, более удобную для обработки экспериментальных результатов. [10]
Однако полиакрилонитрил плохо растворим в полимеризаци-онной системе, тогда как зависимость константы диссоциации полимерного цвиттер-иона от его длины получена нами в предположении, что время развития полимерной цепи больше времени кристаллизации. Было естественным проверить полученные выводы в системах, где полимер растворим. Для этого нами была выбрана система метакрилонитрил - триэтилфосфин - диметил-формамид. [11]
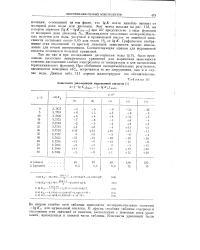 |
Константа диссоциации муравьиной кислоты. [12] |
Так же как и при исследовании диссоциации воды ( § 3), было предложено несколько эмпирических уравнений для выражения зависимости констант диссоциации слабых электролитов от температуры и для вычисления термохимических функций. При обобщении экспериментальных результатов, касающихся поведения C Pi, встречаются те же затруднения, как и в случае воды. Данные табл. 111 хорошо иллюстрируют это обстоятельство. [13]
 |
Константа диссоциации муравьиной кислоты. [14] |
Так же как и при исследовании диссоциации воды ( § 3), было предложено несколько эмпирических уравнений для выражения зависимости констант диссоциации слабых электролитов от температуры и для вычисления термохимических функций. При обобщении экспериментальных результатов, касающихся поведения C0pi, встречаются те же затруднения, как и в случае воды. Данные табл. 111 хорошо иллюстрируют это обстоятельство. [15]
Страницы: 1 2