Зависимость - константа - скорость - реакция
Cтраница 1
Зависимость константы скорости реакции от ионной силы раствора называют первичным солевым эффектом. [1]
Зависимость константы скорости реакции от ионной силы раствора называют первичным солевым эффектом. Хотя экспериментальные точки удовлетворительно ложатся на теоретические прямые, влияние электролитов на константу скорости реакции носит более сложный характер. [2]
Зависимость констант скорости реакции от температуры для исследованных образцов в координатах уравнения Аррениуса представлена на рисунке. [3]
Зависимость константы скорости реакции К от температуры t для ряда реакций приведена в табл. 4.6 Рассмотреть возможность описания функции Kf ( t) уравнением Аррениуса К - К0е - RT, где К0 - предэкспоненциалъный множитель; Е - энергия активации; Т - абсолютная температура; R - универсальная газовая постоянная, и рассчитать коэффициенты уравнения Аррениуса. [4]
Зависимость константы скорости реакции от температуры в большинстве случаев может быть описана полуэмпирическим уравнением С. [5]
Зависимость константы скорости реакции от температуры определяется законом Аррениуса. [6]
Зависимость константы скорости реакции от температуры была предложена Аррениусом и носит название аррениусовской. Теоретически она была обоснована авторами теории активированного комплекса Эйрингом и Поляни. [7]
Зависимость константы скорости реакции от температуры представляет особый теоретический интерес в катализе. [8]
Зависимость константы скорости реакции от температуры подчиняется уравнению Аррениуса. [9]
Зависимость константы скорости реакции силам BTI-I о водородом от обратно. [10]
Зависимость константы скорости реакции k от температуры подчиняется уравнению Аррениуса & Лехр ( - Q / RT), где А и Q - постоянные величины. Поскольку константа скорости Диффузии пропорциональна x2 / t, а не x / t1, как константа скорости реакции, энергия активации диффузии оказывается в 2 раза больше величины Q. Постоянную Q часто называют кажущейся энергией активации. Это различие подробно обсуждалось Рэтлиффом и Пауэллом [35], и неучет его может привести к путанице при сравнении данных. [11]
Зависимость констант скорости реакции хлорангидридов терефталевой и изофталевой кислот с триметилолпропаном и триметилолэтаном от обратной абсолютной температуры находится в соответствии с уравнением Арре-ниуса. В табл. 64 приведены уравнения Аррениуса для этих реакций, а также вычисленные из них кажущиеся энергии активации и предэкспоненци-альные множители. [12]
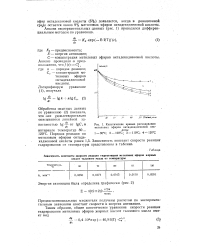 |
Кинетические кривые расходования метиловых эфиров октадекадиеиовой кислоты. 1 90 С. 2 - 100 С. 3 - 110 С. 4 - 120 С. [13] |
Зависимость констант скорости реакции гидрирования от температуры представлены в таблице. [14]
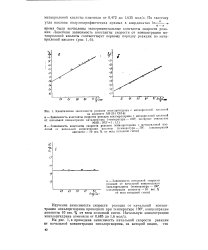 |
Кинетические зависимости реакции эпихлоргидрина с метакриловой кислотой. [15] |
Страницы: 1 2 3 4