Зависимость - концентрация - компонент
Cтраница 2
 |
Зависимость каталитич. константы от рН в логарифмич. координатах. [16] |
Система ур-ний, описывающая кинетику процесса, линейна, если смещение от положения равновесия невелико. Решение системы приводит к зависимостям концентраций компонентов разл. Результатом исследования является спектр времен релаксации, соответствующий числу промежут. [17]
После того как в вышедшем из колонки элюенте появилось анализируемое вещество, на что указывает смещение показаний интерферометра с нулевого положения, уменьшают объемы отбираемых фракций до 0 5 мл и проводят измерения концентрации до тех пор, когда показания интерферометра снова станут нулевыми. Хроматограмму получают, строя график зависимости концентрации компонента ( или показаний детектора) от объема прошедшего через колонку элюента. [18]
Теперь мы рассмотрим уравнение, в котором отражена зависимость концентрации компонентов в исследуемой смеси в любой фракции фильтрата от объема фильтрата. [19]
 |
Аппарат для молекулярной перегонки твердых веществ ( по Уотбурну. [20] |
При молекулярной перегонке отсутствует точно определяемая температура кипения. Идентификацию компонентов дистиллята проводят только химическим путем. Можно вычертить так называемую кривую элиминации; эта кривая изображает зависимость концентрации выделяемого компонента от температуры, при которой его собирают. [21]
 |
Аппарат для молекулярной [ IMAGE ] Прибор для. [22] |
При молекулярной перегонке отсутствует точно определяемая температура кипения. Идентификацию компонентов дистиллята проводят только химическим путем. Можно вычертить так называмую кривую элиминации; эта кривая изображает зависимость концентрации выделяемого компонента от температуры, при которой его собирают. Вид кривой зависит от перегоняемого вещества; она имеет максимум при определенной температуре. Положение максимума зависит от так называемой дистилляционной способности вещества и продолжительности перегонки. [23]
Результаты теории кинетики открытых систем недавно были использованы для изучения конкретной биохимической системы, осуществляющей разложение глюкозы на двуокись углерода и воду. Была разработана упрощенная схема этой реакции [4], включающая 21 стадию, для описания которых нужно соответствующее число уравнений. С помощью цифровой вычислительной машины были обработаны необходимые данные и получены графики зависимости концентраций компонентов от времени; результаты оказались вполне удовлетворительными и подтвердили качественные представления о взаимодействиях между частями этой системы. Кроме того, стало ясно, какие большие усилия требуются для разрешения такой проблемы. [24]
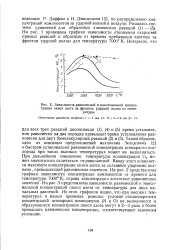 |
Зависимость равновесной и максимальной концентрации окиси азота за фронтом ударной волны от температуры. [25] |
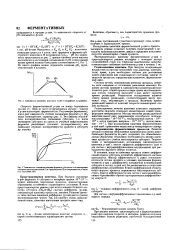
Таким образом, одно из основных предположений механизма Зельдовича [2] о быстром установлении равновесной концентрации атомарного кислорода при таких высоких температурах может не выполняться. При дальнейшем повышении температуры концентрация 02 может значительно отличаться от равновесной. Ввиду этого появляется максимум концентрации окиси азота за сильными ударными волнами, превышающий равновесные значения. На рис. 2 представлены графики зависимости концентрации компонентов от времени для температуры 7000 К; справа концентрации достигают равновесных значений. На рис. 3 представлены зависимости равновесной и максимальной концентраций окиси азота от температуры для двух начальных давлений. Из этих графиков видно, что при высоких температурах и малых временах реакции условие стационарности концентраций атомарных компонентов ( N и О) не выполняется и образующиеся концентрации окиси азота могут в 2 - 3 раза и более превышать равновесные концентрации, соответствующие заданным условиям. [26]
 |
Графики распределения концентраций са компонентов поперек пограничного слоя.| Зависимости концентраций саа компонентов на обтекаемой поверхности от безразмерного времени т. [27] |
Представляют интерес поля концентраций компонентов в пограничном слое для различных моментов времени. На рис. 7.7.3 приведены графики концентраций поперек пограничного слоя для СО2 ( кривые 1 2 3) к для кислорода ( кривые 1, 2, 3) в различные моменты времени. Здесь кривые 1, Г; 2, 2; 3, 3 отвечают тем же моментам времени и тем же значениям безразмерных параметров, что и кривые 2 3 4 на рис. 7.7.2 соответственно. Видно, что химическая реакция локализуется в узкой зоне внутри пограничного слоя - во фронте горения ( кривые 2, 3), который вначале продвигается в сторону свежей смеси, а затем стабилизируется на некотором фиксированном расстоянии от нагретой поверхности. На рис. 7.7.4 приведены зависимости концентраций компонентов на поверхности от времени протекания процесса. Кривая 1 здесь соответствует концентрации СО, 2 - концентрации углекислого газа СО2 3 - концентрации кислорода. Видно, что концентрации компонентов на поверхности довольно быстро выходят на свои асимптотические значения. Этот результат подтверждает сделанный ранее вывод о том, что при 8 - 380 реализуется квазиравновесный режим протекания гомогенной химической реакции. [28]
Страницы: 1 2