Зависимость - логарифм - скорость
Cтраница 3
 |
Кривые зависимости потери в весе от времени для графита при 300. [31] |
Значения скоростей окисления при различных температурах представлены в таблице, а зависимость логарифма скорости от 1 / 7 приведена на рис. 5, причем соответствующие величины энергии активации даны в подписи к рисунку. [32]
 |
Определение порядка реакции. [33] |
Определяя скорость реакции при различных концентрациях реагирующих веществ и строя график зависимости логарифма скорости реакции от логарифма концентрации, определяют наклон полученной прямой, который будет представлять собой порядок реакции относительно вещества, концентрация которого изменялась. [34]
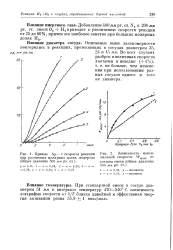
Если теперь определить скорость реакции при различных значениях концентраций реагирующих веществ и построить график зависимости логарифма скорости реакции от логарифма концентрации ( рис. 19), то должна получиться прямая линия. Если точки не ложатся на прямую при заведомо надежных экспериментальных данных, то это означает, что реакция является сложной и выражение скорости ее не имеет определенного порядка. [35]
 |
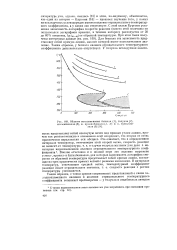
Кривые Д / - t скорости реакции при различных молярпых долях водорода ( общее давление 500 мм рт. ст..| Зависимость максимальной скорости WMaKC от состава смеси ( общее давление 500 мм рт. ст. [36] |
При стандартной смеси в сосуде диаметром 51 мм в интервале температур 470 - 540 С зависимость логарифма скорости от 1 / Т близка линейной и эффективная энергия активации равна 55 8 1 ккал / молъ. [37]
 |
Области воспламенения бензола ( /, толуола ( 2. [38] |
Вполне отчетливо и в полной мере это явление выражено у этил -, пропил - и бутилбензолов, для которых зависимость логарифма скорости от обратной температуры представляет собой кривые линии, состоящие из трех практически прямых ветвей с разными наклонами. [39]
 |
Зависимость скорости разложения муравьиной кислоты над ПАН-1 и ПАН-2 от температуры. [40] |
Так как изменение скорости разложения муравьиной кислоты с ростом температуры определялось нами в одном непрерывном опыте при ступенчатом повышении температуры, постоянной скорости подачи кислоты в реактор и сравнительно небольших глубинах превращения ( от 1 до 10 %), то энергия активации изученной реакции может быть определена из зависимости логарифма скорости разложения кислоты от обратной абсолютной температуры. Рассчитанные по этим графикам энергии активации составляют для ПАН-1 и ПАН-2 соответственно 21 и 25 ккал. Следует отметить, что наблюдаемое повышение активности ПАН-1 и ПАН-2 от опыта к опыту мало сказывается на энергии активации. Так, в опытах 6 и 7 с ПАН-2 энергия активации процесса практически оставалась без изменения. [41]
Значения скоростей окисления при различных температурах приведены в таблице. Зависимость логарифма скорости от 1 / Т показана на фиг. [42]
Зависимость логарифма скорости от обратной температуры представляет собой ярямую линию, по наклону которой определяют эффективную энергию активации протекающего процесса. [43]
На кривых, построенных в полулогарифмических координатах, в катодном процессе наблюдается предельный ток, который носит название предельного тока химической реакции. Зависимость логарифма скорости анодного процесса от перенапряжения ( или потенциала электрода) линейна и описывается уравнением, аналогичным уравнению Тафеля. [44]
На рис. 4 - 12 представлена объемная скорость выгорания углерода из высокозольного материала, деленная на концентрацию кислорода в окружающей частицу среде в зависимости от Т-1 при различных первоначальных плотностях углерода для некоторых значений степеней выгорания. Видно, что зависимость логарифма скорости выгорания углерода, разделенная на концентрацию кислорода, от Т-1 лри различных ро аппроксимируется прямолинейными зависимостями. Следовательно, процесс выгорания углерода из высокозольного материала при названных температурах подчиняется закону Аррениуса. [45]
Страницы: 1 2 3 4 5