Зависимость - электродный потенциал
Cтраница 1
Зависимость электродного потенциала ( см.) электрода, обратимого по отношению к катионам ( например, металла), от активности [15] ионов в растворе описывается уравнением Нернста. [1]
 |
Гальваническая пара для измерения потенциала электрода. [2] |
Зависимость электродного потенциала от активности ионов, относительно которых обратим электрод, позволяет определить их равновесную концентрацию в растворе, а также определить коэффициент активности электролита. Определение активности ионов методом измерения электродного потенциала называется и о н о-м е т р и е и. Этим методом определяют также произведение растворимости труднорастворимых электролитов, степень и константы диссоциации слабых электролитов. [3]
Зависимость электродных потенциалов от концентрации широко используют для определения многих чрезвычайно важных констант: произведения растворимости, константы нестойкости, ионного произведения воды, а также для нахождения концентрации ионов водорода в водных растворах. [4]
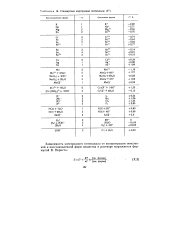 |
Стандартные электродные потенциалы (. [5] |
Зависимость электродного потенциала от концентрации окисленной и восстановленной форм вещества в растворе выражается формулой В. [6]
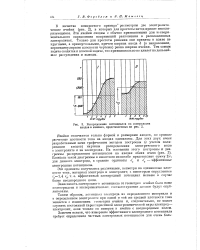 |
Распределение потенциалов на поверхности анодов в ячейках, представленных на 2. [7] |
Зависимость электродного потенциала от геометрии ячейки была нами подтверждена и экспериментально; соответствующие данные будут опубликованы. [8]
Однако зависимость электродного потенциала от содержания стекла в исследованных материалах носит экстремальный характер. Дальнейшее увеличение стекла в образцах влечет за собой частичный переход геля в раствор щелочи, что вызывает открытие пор и доступ коррозионной среды к металлической составляющей образцов. [9]
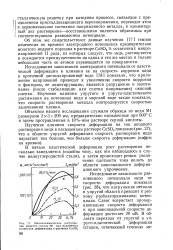 |
Механохимическое растворение медного сплава Ml при различных скоростях деформации в растворе CuSO4. [10] |
Исследования зависимости электродного потенциала от пластической деформации и влияния ее на скорость коррозии меди в проточной дистиллированной воде [78] показали, что приложение напряжений приводит к увеличению скорости коррозии и фактором, ее лимитирующим, является разрушение и залечивание ( после стабилизации или снятия напряжения) окисной пленки. Изучение влияния упругого и упруго-пластического растяжения на потенциал меди в морской воде также показало, что скорость растворения металла контролируется скоростью залечивания пленки. [11]
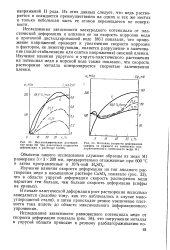 |
Механохимическое растворе-ние меди Ml при различных скоростях деформации в растворе CuSO4.| Влияние скорости деформации ( цифры на кривых на изменение квазиравновесного потенциала меди Ml. [12] |
Исследования зависимости электродного потенциала от пластической деформации и влияния ее на скорость коррозии меди в проточной дистиллированной воде [86] показали, что приложение напряжений приводит к увеличению скорости коррозии и фактором, ее лимитирующим, является разрушение и залечивание ( после стабилизации или снятия напряжения) окисной пленки. Изучение влияния упругого и упруго-пластического растяжения на потенциал меди в морской воде также показало, что скорость растворения металла контролируется скоростью залечивания пленки. [13]
Уравнения выражают зависимость электродных потенциалов от активностей ионов и соотношения между активностями ионов, находящихся в равновесии с твердой фазой; активности ионов выделены фигурными скобками. [14]
Некоторые соображения о зависимости электродных потенциалов от диэлектрической постоянной ( ДП) растворителя будут изложены ниже. [15]
Страницы: 1 2 3 4