Определение - константа - диссоциация - кислота
Cтраница 1
Определение константы диссоциации кислоты Кг основано на измерении оптической плотности и рН серии растворов, содержащих ионы НХ - и Хг в определенном мольном отношении. [1]
Для определения констант диссоциации кислот могут быть применены две цепи: цепи, содержащие буферные растворы, и цепи, не содержащие буферных растворов. [2]
Для определения констант диссоциации кислот могут быть применены лепи, содержащие и не содержащие буферных растворов. [4]
Другим методом определения констант диссоциации кислот в различных растворителях можно считать эмпирический метод, например метод Грюнвальда, и др. 28 29, разработанный для смесей этиловый спирт - вода. [5]
Кондуктометрическая методика определения констант диссоциации кислот не дает возможности отличать ионные пары от неионизированных кислот, тогда как спектрофотометр и я в ультрафиолетовой или видимой области спектра, как лравило, не позволяет отличать ионные пары от свободных ионов. Поэтому в растворителях рассматриваемого класса значения р / Са, определенные этими методами, не совпадают. Это характерно вообще для всех случаев, когда степень диссоциации ионных пар мала. [6]
Можно ли для определения констант диссоциации кислот и оснований использовать гальванический элемент, состоящий из стеклянного и хлорсереб-ряного электродов. [7]
Метод применим к определению констант диссоциации кислоты или основания любой кислотно-основной пары. Необходимость отличия спектров кислоты и сопряженного основания ограничивает применение метода системами, в которых кислотная ( или основная) функция выполняется хромофором или его частью. Тем не менее область применения метода весьма широка, поскольку в нем используются очень малые концентрации и практически не возникает трудностей из-за плохой растворимости веществ. [8]
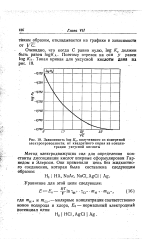 |
Зависимость log Kc, полученного из измерений электропроводности, от квадратного корня из концентрации уксусной кислоты. [9] |
Метод электродвижущих сил для определения константы диссоциации кислот впервые сформулирован Гар-недом и Элерсом. [10]
В этом заключается принцип индикаторного метода определения константы диссоциации кислоты. [11]
Эти методы ( оптическая суперпозиция, оптический сдвиг, определение констант диссоциации кислот и др.) подробно не рассматриваются. [12]
Худ с сотрудниками использовали свои данные также и для определения констант диссоциации кислот. Различные соли вызывают как положительные, так и отрицательные сдвиги порядка 0 1 по абсолютной величине. При интерпретации сдвигов Шулери и Олдер учитывают две противоположные тенденции: разрушение сетки Н - связей в воде и поляризующее действие катионов. [13]
Любую электродную систему, чувствительную к концентрации ионов водорода в растворе, можно, по крайней мере теоретически, применять для определения констант диссоциации кислот и оснований. К этой категории относятся все полуэлементы, в которых участвуют ионы водорода. Однако для решения этой задачи были использованы только некоторые из них. [14]
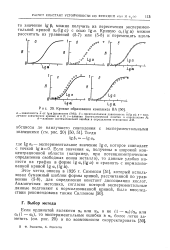 |
Кривые образования комплекса ВА. [15] |
Страницы: 1 2