Определение - константа - нестойкость
Cтраница 1
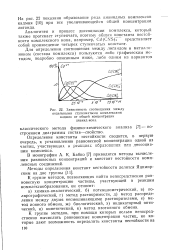 |
Зависимость соотношения между. [1] |
Определение константы нестойкости сводится, в первую очередь, к установлению равновесной концентрации одной из частиц, участвующих в реакциях образования или диссоциации комплекса. [2]
Определение констант нестойкости потенциометрическим методом, как отмечают в ряде статей К. Б. Яцимирский [1] и Н. П. Комарь [2], может быть осуществлено при изучении зависимости потенциала окислительно-восстановительных систем от концентрации комплексообразователей. Здесь, однако, необходимо учитывать, что в нейтральной среде ( или в слабокислой или слабощелочной за счет гидролиза) многие катионы находятся в форме сложных ионов или в форме нерастворимых соединений. Кроме того, электропроводность сантинормальных водных растворов мала и измерение потенциала окислительно-восстановительных систем, особенно до введения комплексо-образователя, не всегда возможно. Следовательно, определение константы нестойкости потенциометрическим методом возможно лишь в том случае, если измерение потенциала окислительно-восстановительных систем производят при различной концентрации комплексообразователя. Отметим, что, согласно литературным данным, большинство ионов образует с одним аддендом несколько комплексов. [3]
Определение констант нестойкости дает возможность не только получить количественные данные относительно устойчивости соединений в растворенном состоянии, но и охарактеризовать их с термодинамической точки зрения. [4]
Определение константы нестойкости относится только к разрушению комплексного иона как слабого электролита. По величине константы нестойкости определяют концентрации катионов металла и лигандов в растворе. [5]
Для определения констант нестойкости методом ионного обмена изучают распределение ионов комплексообразующего элемента, содержащего радиоактивный изотоп, между катионитом и раствором в отсутствие и в присутвии ионов комплексообразователя. [6]
Для определения констант нестойкости существует много методов. [7]
Для определения константы нестойкости комплексных соединений кадмия необходимо иметь раствор с концентрацией соли кадмия около 10 - 7 моль / л и измеряемой скоростью счета около 2000 имп / мин на 1 мл раствора. [8]
Задача определения константы нестойкости сводится к определению концентрации ионов свободного металла и концентрации комплексного иона. Во втором случае катионитом будут поглощаться также только свободные ионы металла, так как по условию заряд образующегося комплекса или равен нулю, или отрицателен. [9]
Обычно определению констант нестойкости и состава комплексов реагентов с металлами предшествует выяснение полярографической характеристики самого реагента, а затем определение наиболее благоприятных условий взаимодействия его с металлами. Для этого часто определяют константы ионизации реагента. [10]
При определении констант нестойкости методом растворимости, при котором требуется найти растворимость соли, вступающей в комплексообразование, при различных концентрациях комплексообразователя, концентрация насыщенного раствора находится так же, как в случае описанного в гл. [11]
При определении констант нестойкости методом растворимости, при котором требуется найти растворимость соли, вступающей в комплексообразование, при различных концентрациях комплексообразователя, концентрация насыщенного раствора находится так же, как в случае описанного в гл. [12]
Подобный метод определения констант нестойкости был предложен Леденом [12] для случаев потенциометрических измерений. [13]
Потенциометрический метод определения констант нестойкости разработан относительно давно и по сей день часто применяется. Для этой цели используются электроды стеклянный, платиновый, а также другие металлические электроды. [14]
Подобный метод определения констант нестойкости был предложен Леденом [12] для потенциометрических измерений. [15]
Страницы: 1 2 3 4