Определение - константа - нестойкость
Cтраница 3
Были сделаны удачные попытки применить ионообменный метод для решения различных качественных задач ( например, определение знака заряда комплексов, валентности ионов, оценка относительной способности ионов к комплексообразованию) и для определения констант нестойкости комплексов. [31]
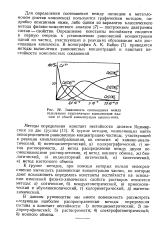 |
Зависимость соотношения между отдельными ступенчатыми комплексами кадмия от общей концентрации цианид-иона. [32] |
Для определения соотношения между лигандом и металло-ионом ( состав комплекса) пользуются графическим методом, подробно описанным ниже, либо одним из вариантов классического метода физико-химического анализа [7] - построением диаграммы состав - свойство. Определение константы нестойкости сводится в первую очередь к установлению равновесной концентрации одной из частиц, участвующих в реакциях образования или диссоциации комплекса. В монографии А. К. Бабко [7] приводятся методы вычисления равновесных концентраций и констант нестойкости комплексных соединений. [33]
Весьма существенной характеристикой комплексного соединения является его константа нестойкости. Определение константы нестойкости окрашенных соединений, образующихся в растворе под влиянием окрашенных реактивов, обычным способом затруднительно, - поэтому константа нестойкости определялась по способу Бабко - Пилипенко, дающему ориентировочные результаты. [34]
Строго говоря, в приведенных выражениях следовало бы писать по концентрации, а активности соответствующих ионов. Однако при определении констант нестойкости применяют растворы с, постоянной ионной сплои, что позволяет полышвптг. Встречающиеся иногда тсрмкнм ( константы диссоциацпч комплекса, константы комплексности, константа закомплексованности являются с i; поп штамп пометил константа нестойкости п пока еще не получили достаточно широкого распространения. [35]
Строго говоря, в приведенных выражениях следовало бы писать не концентрации, а активности соответствующих ионов. Однако при определении констант нестойкости применяют растворы с постоянной ионной силой, что позволяет пользоваться выражениями в приведенной выше форме. Иногда для характеристики устойчивости комплекса служат к о п-станты устойчивости К ( иначе константа образования комплексного соединения) - величины, обратные константам нестойкости: А 1 / К. Встречающиеся иногда термины константы диссоциации комплекса, константы комплексности, константа закомплексованности являются синонимами понятия константа нестойкости и пока ещо не получили достаточно широкого распространения. [36]
Однако эта точка зрения нашла мало сторонников в силу ряда причин практического удобства. Птицына основывается на определении констант нестойкости комплексов, выделенных в твердом состоянии с помощью препаративного метода, и в недостаточной степени учитывает специфику нахождения констант стойкости ( образования) при исследовании комплексообразования в растворах. [37]
На рис. 2.55 приведены типичные 2.55. Зависимость отно - кривые относительного поглощения. Та-сительного поглощения ис - кого вида графики можно использовать следуемого элемента катиони - ддя ОПределения констант нестойкости ra p % V ции добав - графическим методом. [38]
Из ряда констант нестойкости для одного н того же комплекса взято, как правило, только одно, наиболее достоверное значение. Число значащих цифр, приводимых в таблицах, не всегда указывает на действительную точность определения констант нестойкости. [39]
Последнее стало доступным вследствие применения платинового электрода в качестве электрода первого рода по отношению к ионам двухвалентной платины. Позднее было установлено, что палладиевый электрод также может служить электродом первого рода по отношению к ионам двухвалентного палладия и, следовательно, использоваться для определения констант нестойкости палладиевых комплексов. [40]
Известно, что при наложении электрического поля на раствор электролита наблюдается явление электрофореза - перемещение заряженных частиц к соответствующим электродам. Электрофорезом пользуются, например, для определения заряда комплексных ионов, а за последние годы он начал приобретать значение как метод разделения РЗЭ и как метод определения констант нестойкости комплексных соединений. [41]
Так, он считал более логичным обозначать константу нестойкости, отвечающую отщеплению первого иона хлора из иона [ PtCl4 ] 2 через klt а последнего ( четвертого) через &4. Однако эта точка зрения нашла мало сторонников в силу ряда причин практического удобства. Птицына основывается на определении констант нестойкости комплексов, выделенных в твердом состоянии с помощью препаративного метода, и в недостаточной степени учитывает специфику нахождения констант стойкости ( образования) при исследовании комплексообразования в растворах. [42]
Этот метод применим для определения констант нестойкости комплексов, в состав которых входят катионы, восстанавливающиеся на ртутном или неподвижном катоде. Образование комплексного иона при добавлении к раствору лиганда вызывает смещение потенциала полуволны. На основании этого разработаны методы определения констант нестойкости комплексов. [43]
Электровосстановлению на ртутном капающем электроде могут подвергаться не только простые, но также и комплексные ионы металлов. Потенциалы полуволн комплексных ионов металлов смещаются к более отрицательным значениям относительно потенциалов простых ионов. Величина этого смещения является функцией концентрации лигандов, а также устойчивости образующегося комплекса, что позволяет пользоваться полярографическим методом как для определения констант нестойкости комплексов, так и для выяснения их состава. Вполне естественно, что это возможно только при условии, что на сдвиг потенциалов полуволн не влияют другие факторы - необратимость диссоциации комплексов, необратимость их восстановления и др. Правда, случаи необратимого восстановления комплексов встречались до последнего времени в литературе не так часто. [44]
Определение констант нестойкости потенциометрическим методом, как отмечают в ряде статей К. Б. Яцимирский [1] и Н. П. Комарь [2], может быть осуществлено при изучении зависимости потенциала окислительно-восстановительных систем от концентрации комплексообразователей. Здесь, однако, необходимо учитывать, что в нейтральной среде ( или в слабокислой или слабощелочной за счет гидролиза) многие катионы находятся в форме сложных ионов или в форме нерастворимых соединений. Кроме того, электропроводность сантинормальных водных растворов мала и измерение потенциала окислительно-восстановительных систем, особенно до введения комплексо-образователя, не всегда возможно. Следовательно, определение константы нестойкости потенциометрическим методом возможно лишь в том случае, если измерение потенциала окислительно-восстановительных систем производят при различной концентрации комплексообразователя. Отметим, что, согласно литературным данным, большинство ионов образует с одним аддендом несколько комплексов. [45]
Страницы: 1 2 3 4