Определение - константа - равновесие
Cтраница 1
Определение константы равновесия для превращения mpe / n - бутильного катиона в 2-метилпропен особенно важно, так как этот ион является прототипом всех третичных алкильных катионов. [1]
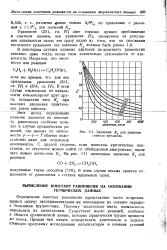 |
Значения AT для реакции синтеза метанола. [2] |
Определение констант равновесия представляет часто встречающуюся задачу; экспериментальное же нахождение их связано нередко с большими трудностями. Поэтому желательно иметь возможность определять их вычислением. [3]
 |
Спектр поглощения гидроперекиси а-тетралина в растворе СС14. Концентрация 0 027. [4] |
Определение константы равновесия затруднено тем, что для нахождения концентрации одного из конформеров необходимо знать коэффициент поглощения соответствующей полосы. В реальных же условиях в растворе всегда присутствуют и транс - и гош-изомеры, что не позволяет рассчитать их концентрации. [5]
Определение константы равновесия является одной из важнейших практических задач химической термодинамики. Если система находится в состоянии равновесия, тем самым дается четкий положительный ответ на вопрос о возможности сохранения неизменных свойств вещества и составляющих его фаз, пока сохраняются равновесные значения состава, давления и температуры в системе. Если система не находится в состоянии равновесия, тем самым указывается на возможность протекания реакции, если в данных условиях скорость последней может быть достаточной. [6]
Определение констант равновесия связано с применением статистических методов. V констант равновесия и для этого измеряется какая-то функция этих констант у, вид которой известен. Проводят К измерений, причем / С N и разность К - N р называется числом статистических степеней свободы. [7]
Определение константы равновесия решением относительно К уравнений связи типа ( XXVI. Эта величина не может быть определена экспериментально, так как в случае, если К конечна, взаимодействие ( IV) не проходит до конца и AmBn не может быть выделено из равновесной смеси. [8]
Определение константы равновесия по правилу летучести может быть рекомендовано в пределах давлений от 4 до 20 ат. С увеличением давления растет взаимное влияние компонентов на распределение их между фазами и особенно сильно оно проявляется в критической области. [9]
Определение константы равновесия фракции С7 по заданным изотермам конденсации заключается в следующем. [10]
Определение констант равновесия этана, пропана, к-бутана при бесконечном разбавлении в системе метан - бутан с помощью газовой хроматографии. [11]
Определение констант равновесия химических реакций по уравнениям ( 111 71) - ( 111 73) называется методом Темкина - Шварцмана. В настоящее время этот метод широко используется для расчета констант равновесия реакций и дает достаточно точные результаты. Это объясняется тем, что теплоты образования ДЯ / 298 и абсолютные энтропии 5298, необходимые для расчета ДЯ298 и ASjgs по уравнению ( 111 71), берутся из справочных таблиц. [12]
Определение константы равновесия кислоты ВН, а также отношения СВ / СВН может быть осуществлено с помощью одного из описанных ранее методов. [13]
Для определения константы равновесия применяются также многие другие экспериментальные методы. [14]
Для определения константы равновесия необходимо изменение д всех коэффициентов ( кроме N) умножить на соответствующие каждой заданной температуре температурные функции, численные значения которых приведены в табл. 2 приложения. [15]
Страницы: 1 2 3 4