Определение - константа - равновесие
Cтраница 2
Для определения констант равновесия необходимо рассматривать изменения свободной энергии веществ в стандартном состоянии. [16]
Для определения константы равновесия / Ci при отсутствии опытных значений или удобных корреляций рекомендуется применять метод, основанный на использовании псевдокритических констант. Значения фугитивности находятся в соответствии с указаниями, приведенными в приложении VI, причем значения fiL и fif приравниваются друг к другу. Этот метод довольно громоздок и требует применения ЭВМ. [17]
Для определения констант равновесия изучают также растворимость солей слабых кислот в сильных кислотах: с ростом кислотности она увеличивается. [18]
Для определения констант равновесия изучают также растворимость солей слабых кислот в сильных кислотах. Растворимость таких солей с ростом кислотности увеличивается. [19]
Для определения константы равновесия ими был использован метод разделения паров. В общем, результаты для этих трехкомпонентных систем показали, что дополнительная полярность, возникающая при образовании водородной связи, возрастает по мере увеличения константы равновесия реакции образования комплекса. [20]
Для определения констант равновесия при давлении насыщения или точке росы можно пользоваться данными, опубликованными в работах Катца и Хачмата [8], Роланда, Смита и Кевелера или из других источников. Выбрать следует те сведения, которые наиболее близко соответствуют составу исследуемой углеводородной смеси. Давление насыщения или точка росы подсчитываются по уравнениям контактного дегазирования, которые приведены в главе IV, по результатам анализа углеводородной смеси и выбранным значениям констант равновесия. Давление, для которого определяются ( по литературным данным) константы равновесия, не учитывается. [21]
Однако определение константы равновесия по уравнениям ( 3) и ( 4) оправдывает себя только до давлений не выше 3 - 4 ат. [22]
Для определения константы равновесия компонента СбН высшие или С6Н14 высшие необходимо иметь следующие данные о свойствах остатка: фракционной разгонке остатка и его плотности или молекулярной массе остатка и его плотности. [23]
Для определения константы равновесия КНА был проведен следующий опыт. [24]
Для определения константы равновесия КР необходимо знать суммарное давление Р смеси газов в момент равновесия, а также степень диссоциации а. Обе эти величины могут быть измерены с помощью видоизмененного прибора В. Если обозначить р парциальное давление недиссоциированных молекул 12 и р2 парциальное давление атомов I в состоянии равновесия, то суммарное давление, согласно определению ( стр. Суммарное давление Р при равновесии выражается общим числом молей компонентов, содержащихся в данной смеси; согласно уравнению ( 13), п 1 ос. [25]
Для определения констант равновесия углеводородных смесей, в том числе и содержащих водород, может быть рекомендован метод Чао и Сидера ( см. раздел VI. Вблизи критической точки удобно пользоваться методом Меры, Брауна и Тодоса [ уравнение ( VI. Бенедикта - Вебба - Рубина ( приложение V) или упрощенными диаграммами Эдмистера и Руби [130, 131], причем результаты имеют высокую точность. Эти методы позволяют рассчитывать значения K. [26]
Для определения константы равновесия диссоциации окисла металла в пламя, питаемое горючей смесью определенного состава, вводится раствор соли металла известной концентрации. Парциальное давление паров металла РШ в пламени определяется на основании спектроскопического измерения интенсивности резонансных линий атомов металла. Парциальное давление паров окислов РШО может быть вычислено в предположении, что реакция Ме -) - 0 МеО есть единственная, в которой принимает участие металл в пламени. [27]
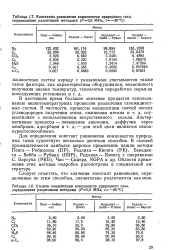
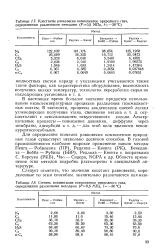
Для определения констант равновесия компонентов природных газов существует несколько десятков способов. В газовой промышленности наиболее широкое применение нашли методы Пенга - Робинсона ( ПР), Редлиха - Квонга ( РК), Бенедикта - Вебба - Рубина ( БВР), Редлиха - Квонга с поправками С. Барсука ( РКБ), Чао - Сидера, NGPA и др. Области применения этих методов подробно рассмотрены в специальной литературе. [29]
Страницы: 1 2 3 4