Определение - константа - скорость - реакция
Cтраница 1
Определение константы скорости реакции нами производилось в приборе с фильтром Шотта № 3 диаметром 4 см; кислород поступал с оптимальной скоростью 1.2 л в 1 мин. [2]
Для определения константы скорости реакции ( 43); равной 4 104 л - моль 1 с 1 при 250 С в бензоле, использован метод конку - - рирующих реакций. [3]
Для определения константы скорости реакции может быть предложено несколько способов. [4]
Для определения констант скорости реакций радикалов необходимо каким-либо способом создать нестационарную концентрацию радикалов и по хемилюминесценции зарегистрировать кинетику установления стационарного режима. [5]
Для определения констант скорости реакции озона с соединениями, содержащими элементоорганические кратные связи, была использована описанная выше методика. [6]
Методы определения констант скоростей реакций описаны ниже в главе Скорость химических реакций ( стр. [7]
Рассмотрим примеры определения констант скорости реакции первого и второго порядков. [8]
Конечно, для определения констант скоростей реакции диазо-тирования метод, примененный в наших исследованиях, а также колориметрический метод не обладают достаточной точностью. [9]
Таким образом, для определения констант скоростей реакций, механизм которых установлен и которые можно изучать в условиях псевдопервого порядка по концентрации А, достаточно знания относительных концентраций атомов. Остается широкий класс реакций более сложных порядков, например ре-комбинационные процессы с участием двух атомов, для которых требуется определить абсолютные концентрации атомов. Знание абсолютных концентраций атомов необходимо для анализа реакций, механизм которых неизвестен, для получения информации о стехиометрии реакции. [10]
Целью настоящего исследования является определение константы скорости реакции ( 1) в системе НС1О4 - НС1О3 - НС1 - Ь О при температуре 20 С. [11]
Меченые атомы делают возможным определение констант скоростей реакций при равновесии. Обычно константы скорости определяли в условиях, далеких от равновесия, и никаких данных о том, что кинетика реакции не изменяется при приближении к равновесию, до сего времени не было. [12]
Существуют значительные возможности для определения констант скоростей реакций свободных радикалов в струевых разрядных установках. До сих пор детально исследованы только реакции радикалов ОН, CIO, BrO, NF2 и намного меньше изучены реакции радикала CN. [13]
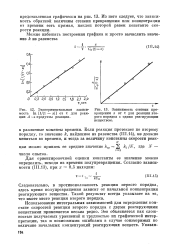 |
Экспериментальная зависимость In [ 1 / ( 1 - х ] от т для реакции А - продукты реакции.| Зависимость степени превращения х от т для реакции второго порядка с одним реагирующим веществом. [14] |
Использование интегральных зависимостей для определения констант скоростей реакции второго порядка с двумя реагирующими веществами применяется весьма редко. Это объясняется как сложностью получаемых уравнений и трудностью их графической интерпретации, так и возможными ошибками в случае соизмеримых по величине начальных концентраций реагирующих веществ. [15]
Страницы: 1 2 3 4