Определение - концентрация - ион - водород
Cтраница 3
При условии, что Е известно, это уравнение может служить основой для определения концентрации ионов водорода в неизвестном растворе. [31]
Эта номограмма также позволяет находить интервалы показателей титрования фенолфталеина для каждого заданного значения допустимой ошибки в определении концентрации ионов водорода. Для этого нужно: из соответствующей ( заданному значению ошибки в определен. [32]
Приготовленные указанным способом растворы индикаторов вполне пригодны для применения их в обычных целях, но если они должны служить для определения концентрации ионов водорода в растворах с малой буферной емкостью, их надо предварительно привести к концентрациям ионов водорода, соответствующим рН середины интервала перехода их окрасок ( например, бромфеноловый синий-3 80; бромкрезоловый пурпурный-5 80; бромтимоловый синий - 6 80; феноловый красный-7 60) [ W. Те же авторы отмечают, что концентрация ионов водорода в растворах индикаторов заметно изменяется при хранении этих растворов в стеклянной посуде; в сосудах из обыкновенного стекла она понижается, в сосудах из стекла пайреск и в парафинированных внутри колбах она повышается. [33]
Приготовленные указанным способом растворы индикаторов вполне пригодны для применения их в обычных целях, но если они должны служить для определении концентрации ионов водорода в растворах с малой буферной емкостью, их надо предварительно привести к концентрациям ионов водорода, соответствующим рН середины интервала перехода их окрасок ( например, бромфеноловый синий-3 80; бром-крезоловы Й пурпурный-5 80; бромтимоловый синий-6 80; феноловый красный-7 60) [ W. Те же авторы отмечают, что концентрация ионов водорода в растворах индикаторов заметно изменяется при хранении этих растворов в стеклянной посуде; в сосудах из обыкновенного стекла она понижаетса, в сосудах из стекла пайреск и в парафинированных внутри колбах она повышается. [34]
В настоящем задании предлагается количественно изучить равновесие с участием ионов водорода и гидроксида и характер смещения равновесия при изменении условий. Для определения концентрации ионов водорода и гидроксида ис - пользуется специальный прибор, измеряющий концентрацию ( активность) ионов водорода в единицах рН, так называемый рН - метр. [35]
Как видим, первая константа диссоциации значительно больше второй, а вторая больше третьей. При определении концентрации ионов водорода в растворе многоосновной кислоты в большинстве случаев принимают во внимание лишь первую ступень диссоциации, если константа ее не меньше чем в 1000 раз больше константы диссоциации последующей ступени. [36]
Ввиду того что определение концентрации ионов водорода ( концентрации ионов гидроксония) имеет для различных целей совершенно исключительное значение, здесь будут коротко рассмотрены наиболее важные из этихметодов. Все описываемые методы позволяют определить кажущуюся концентрацию ионов водорода, а не истинную, поскольку истинная отличается от кажущейся. Согласно сказанному на стр. [37]
Хингидрон является очень важной системой окисления - восстановления. Он применяется при погенциометрическом определении концентрации ионов водорода хингидронным электродом. [38]
Поскольку слабые кислоты диссоциируют в воде лишь частично, слабая кислота, например уксусная, создает в водном растворе меньшую концентрацию ионов водорода, чем полная концентрация добавляемой в раствор кислоты. В таких случаях для определения концентрации ионов водорода и проведения связанных с этим расчетов приходится обращаться к выражению для константы диссоциации слабой кислоты. Чтобы пояснить сказанное, вычислим рН 0 0100 М раствора уксусной кислоты. [40]
Сурьмяный электрод Sb / Sb2O, - электрод второго рода, составленный из металла и его малорастворимой окиси. Этот электрод используется для определения концентрации ионов водорода, так как металлический электрод в присутствии своего малорастворимого оксида выполняет функции водородного электрода. [41]
Одним из специальных видов анализа, счень часто выполняемого потенциометрическим методом, является определение концентрации ионов водорода. Теория этого метода совпадает с теорией определения катионов металла, поскольку водород в этом случае рассматривается как металл. [42]
Большинство индикаторов, принадлежащих к классу азо-красителей, а также конго красный, совершенно неприменимы для измерения рН в белковых растворах. Фта-леины и сульфофталеины реагируют с нерасщепленными белками, но е реагируют с продуктами их распада и поэтому могут быть употреблены для определения концентрации ионов водорода, обусловленной продуктами распада белков. Для определения рН с индикаторами в белковых средах существует следующее правило: чем проще состав индикатора, тем меньше его белковая ошибка, тем более он пригоден для работы. [43]
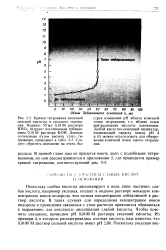
В результате получилась номограмма ( рис. 1), позволяющая для различного оформления титрования с применением в качестве индикатора фенолфталеина находить графическим путем величины ошибок в определении концентрации водородных ионов для каждого заданного значения показателя титрования. Для этого необходимо из соответствующей заданному показателю титрованию точки на оси ординат провести прямую линию, параллельную оси абсцисс, до точки пересечения с кривой / / и из этой точки опустить перпендикуляр на ось абсцисс, после чего из точек пересечения этого перпендккуляра с кривыми о, и и с опустить перпендикуляры на ось ординат, где нанесены значения относительных ошибок в определении концентрации ионов водорода и абсолютных ошибок в определении рН растворов в соответствукших масштабах. [44]
Определение функции кислотности необходимо при работе с Н - формами сильнокислотных катионитов. При сорбции лабильных органических веществ находят очень широкое использование слабокислотные и низкоосновные иониты, а также солевые формы сильнокислотных ионитов. Индикаторный метод определения концентрации ионов водорода в фазе ионита является универсальными имеет то безусловное преимущество, что необходимая концентрация индикатора на несколько порядков меньше концентрации других обменивающихся ионов и вследствие этого она может быть исключен а из рассмотрения при описании ионообменного равновесия. [45]
Страницы: 1 2 3 4