Определение - коэффициент - активность
Cтраница 2
Для определения коэффициентов активности - у, ионов уксусной кислоты следует определить у0 хлористого водорода, уксуснокислого серебра и хлористого серебра. [16]
Рассмотрим определение коэффициентов активности по давлению пара растворенного вещества: например, коэффициентов активности хлористого водорода в водном растворе. [17]
Для определения коэффициентов активности у, ионов уксусной кислоты следует определить у хлористого водорода, уксуснокислого серебра и хлористого серебра. [18]
Рассмотрим определение коэффициентов активности водного раствора неэлектролита в присутствии электролита, например, определение коэффициентов активности фенола, находящегося в водном солевом растворе, принимая за стандарт ту активность, которую имеет фенол, находящийся в чистой воде. [19]
Для определения коэффициента активности твердого растворенного вещества целесообразно выбрать второе стандартное состояние. [20]
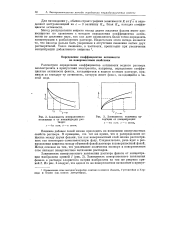 |
Зависимость поверхностного натяжения а от концентрации раствора.| Зависимость величины адсорбции от концентрации. [21] |
Рассмотрим определение коэффициентов активности водного раствора неэлектролита в присутствии электролита, например, определение коэффициентов активности фенола, находящегося в водном солевом растворе, принимая за стандарт ту активность, которую имеет фенол, находящийся в чистой воде. [22]
Метод определения коэффициентов активности путем экстракции растворов инертным газом не требует ни предварительной калибровки хроматографических детекторов, ни трудоемкой подготовки аппаратуры. В упомянутых работах он характеризуется как наиболее точный и привлекательный благодаря своей простоте, надежности и возможности распространения на летучие растворители. [23]
Метод определения коэффициента активности по изменению упругости паров растворителя над раствором солей различной концентрации в конечном итоге также учитывает свободную энергию разведения. Поэтому если не связывать результаты подсчетов с формальными выводами о сверхидеальных свойствах растворов, то расчеты коэффициентов активности не приводят к ошибочным результатам. [24]
Метод определения коэффициентов активности и др. термодинамических величин для углеводородов С4 ( бутан, бутен-1, цис - и гра с-бутены-2, бутадиен) в фурфуроле и констант равновесия для системы и-бутан-н-додекан. [25]
Результаты определений коэффициентов активности с помощью метода изопиестических измерений давления пара весьма точны и хорошо совпадают с данными, полученными путем измерений электродвижущих сил. [26]
 |
Значения Y. ввод - компенсирующих напряжений. [27] |
Возможность определения коэффициентов активности ионов одного вида на основе измерения потенциалов электрокапиллярного максимума ртути обсуждалась также Счастны и Стра-фельда [74] и Трассата с сотрудниками [75, 76]; статья [68] авторам этих публикаций была, по-видимому, неизвестна. В работе [74] сделана попытка определить коэффициенты активности хлорид-ионов в водных растворах хлорида калия, причем авторы не делают различия между реальной и химической активностью. Цепи, изучавшиеся авторами, содержали жидкостные границы, и в экспериментально найденные потенциалы нулевого заряда ртути вводились поправки на диффузионный потенциал, которые рассчитывали по уравнению Гендерсона. [28]
При определении коэффициентов активности косвенными методами их оценивают по изменению свойств растворителя, а это не дает возможности различать изменения свойств, вызванных катионом, от изменения свойств, вызванных анионом. [29]
При определении коэффициента активности по второму приближению Дебая и Хюккеля правильно, как указано выше, все расчеты относить к сольватированным ионам. Следовательно, некоторую часть растворителя нужно рассматривать как прочно связанную с ионами растворенного вещества и, таким образом, не выполняющую функции растворителя. Будем считать, что с одним молем растворенного, полностью диссоциированного, электролита связано h молей растворителя. Если один моль электролита распадается на v молей катионов и v молей анионов, то с ними связано v / z v / i молей растворителя. [30]
Страницы: 1 2 3 4