Определение - коэффициент - активность
Cтраница 3
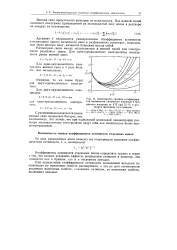 |
Зависимость средних коэффициентов активности хлористого водорода и бромистого водорода от Ym при 25 С в растворах щелочных галогенидов. [31] |
При определении коэффициентов активности косвенными методами их оценивают по изменению свойств растворителя, а это не дает возможности различать изменения свойств, вызванных катионом, от изменения свойств, вызванных анионом. [32]
При определении коэффициентов активности косвенными методами мы оцениваем их по изменению свойств растворителя, а это не дает возможности различать изменения свойств, вызванных катионом, от изменения свойств, вызванных анионом. [33]
При определении коэффициентов активностей жидких углеводородов за стандартное состояние для химического потенциала было принято состояние данного углеводорода в чистом виде при тех же р и Т, что и раствор, тогда как при определении коэффициента - активности метана в жидкой фазе ( уравнение IIL8) за стандартное состояние принималось состояние бесконечного разбавления, экстраполированное на концентрацию метана, равную единице. Этим объясняется тот факт, что коэффициент активности метана в жидкой фазе меньше единицы, а коэффициент активности жидкого углеводорода в той же фазе больше единицы. [34]
Рассмотрим подробнее определение коэффициентов активности на основании измерения давления пара и измерений температуры замерзания растворов. [35]
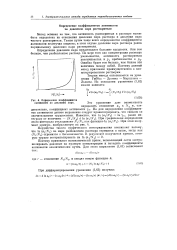 |
Определение коэффициентов активности по давлению пара. [36] |
Но для определения коэффициентов активности данное выражение следует проинтегрировать, что связано со значительными трудностями. [37]
Рассмотрим подробнее определение коэффициентов активности на основании измерения давления пара и измерений температуры замерзания растворов. [38]
Если для определения коэффициентов активности отдельных конов [41] основываться на теорию ионной гидратации, то цифры получаются несколько иные. [39]
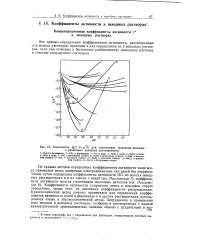 |
Зависимость Igy от УГП для галогенидов щелочных металлов в различных неводных растворителях. [40] |
Все приемы определения коэффициентов активности, рассмотренные для водных растворов, пригодны и для определения их в неводных растворах, если они отнесены к бесконечно разбавленному неводному раствору в качестве стандартного состояния. [41]
Ввиду невозможности определения коэффициентов активности окисленной и восстановленной форм при одновременном их присутствии последним слагаемым в уравнении ( 1) пренебрегают, хотя для многовалентных ионов ( например, в фер-рицианидной-ферроцианидной системе) величина его уже при ионной силе порядка 0 01 может составлять несколько десятков милливольт. [42]
Экспериментальные методы определения коэффициентов активности и методы их теоретического расчета известны из курса физической химии. [43]
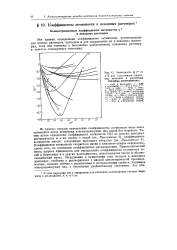 |
Зависимость lg у от Vт для галогеиидов щелочных металлов в различных неводных растворителях. [44] |
Все приемы определения коэффициентов активности, рассмотренные для водных растворов, пригодны и для определения их в неводных растворах, если они отнесены к бесконечно разбавленному неводному раствору в качестве стандартного состояния. [45]
Страницы: 1 2 3 4