Определение - вириальный коэффициент
Cтраница 2
Практическое использование вириального уравнения состояния ( 8 - 40) - ( 8 - 42) наталкивается на трудности, связанные не только с определением старших вириальных коэффициентов чистых компонент, что уже отмечалось ранее, но главным образом с вычислением перекрестных вириальных коэффициентов, для определения которых необходимо иметь сведения о потенциале взаимодействия разнородных частиц. [16]
Вц, Сх и В, С - функции температуры, определяемые по опытным данным т) и Я методом Кейса, обычно применяющимся для определения вириальных коэффициентов из РУГ-данных; Р ( Р - 1): 100 - избыточное приведенное давление в барах. [17]
Для реальных газов достаточно большой плотности уравнение Майера - Боголюбова дает приемлемую точность лишь при наличш; большего числа членов вириального ряда. В определении соответствующих вириальных коэффициентов большое значение имеют экспериментальные исследования теплофизических свойств тех газов, для которых составляются такие уравнения состояния. [18]
Для определения вириальных коэффициентов используют различные методы. Рассмотрим кратко один из них - определение вириальных коэффициентов по результатам измерения удельных объемов газа. [19]
Пример родственного метода был дан в работе Питцера и Уэлтнера [2156], которые исследовали теплоемкость паров метанола. Данные о теплоемкости они использовали для определения вириальных коэффициентов и применили вычисленные значения четвертого вириального коэффициента для доказательства присутствия в парах метанола тетрамеров. Соответствующей интерпретации коэффициента В в этой работе не дано. [20]
Для определения вириальных коэффициентов используются различные методы. Рассмотрим кратко один из них - определение вириальных коэффициентов по результатам измерения удельных объемов газа. [21]
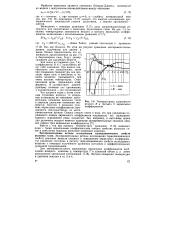 |
Температурные зависимости второго В и третьего С вириальных коэффициентов. [22] |
Экспериментальные методы исследования термодинамических свойств реальных веществ сводятся к определению вириальных коэффициентов уравнения состояния и расчету термодинамических свойств исследуемого вещества с помощью полученного уравнения состояния и дифференциальных уравнений термодинамики. [23]
В главе, подготовленной данным автором для книги, посвященной преимущественно экс-перментальным аспектам химической термодинамики, рассмотрен ряд исследований объемных свойств газовых смесей. Приводится также описание исследовательских работ в области вириального уравнения состояния, экспериментальной методики определения вириальных коэффициентов, расчета перекрестных вириальных коэффициентов, механизма ассоциации паровой фазы, третьих вириальных коэффициентов и избыточных функций. [24]
В главе, подготовленной данным автором для книги, посвященной преимущественно экс-перментальным аспектам химической термодинамики, рассмотрен ряд исследований объемных свойств газовых смесей. Приводится также описание исследовательских работ в области вириалыюго уравнения состояния, экспериментальной методики определения вириальных коэффициентов, расчета перекрестных вириальных коэффициентов, механизма ассоциации паровой фазы, третьих вириальных коэффициентов и избыточных функций. [25]
В книге рассмотрены хроматографические методы изучения термодинамики растворов, а также другие неаналитические применения газовой хроматографии. В частности, освещены вопросы, имеющие большое теоретическое и практическое значение: определение коэффициентов активности при бесконечном разбавлении, определение вириальных коэффициентов в уравнении газового состояния и коэффициентов диффузии, изучение сорбционных свойств адсорбентов и катализаторов. [26]
Большинство других термодинамических величин превращается в идеальногазовые величины при нулевом давлении, и в отличие от jj, они не могут дать информацию по вириальным коэффициентам. Например, коэффициент Джоуля при изменении давления ( или плотности) стремится к нулю по квадратичной зависимости при давлении, стремящемся к нулю, и поэтому почти бесполезен для определения вириальных коэффициентов. [27]
 |
Определение коэффициента С по экспериментальным данным. [28] |
Последовательно применяя описанную выше процедуру, можно определить необходимое число вириальных коэффициентов. Однако следует заметить, что при обычной точности экспериментальных значений удельных объемов 0 2 % уже при определении четвертого или пятого вириального коэффициента разброс точек на соответствующем графике становится очень большим так что невозможно провести сколько-нибудь надежную линию изотермы. Это и является пределом определения вириальных коэффициентов. [29]
Как было показано в разд. Джоуля T ( dTldV) E находится в квадратичной зависимости от давления ( плотности) и стремится к нулю при приближении давления к нулю. Поэтому он не очень полезен для определения вириальных коэффициентов и почти никогда не использовался с этой целью. [30]
Страницы: 1 2 3