Определение - дипольный момент
Cтраница 1
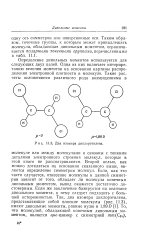 |
Два изомера дихлорэтилена. [1] |
Определение дипольных моментов используется для следующих двух целей. Одна из них включает интерпретацию величин моментов на основании картины распределения электронной плотности в молекуле. [2]
Определение дипольных моментов имеет существенное значение в тех случаях, когда необходимо установить симметрию больших органических молекул, которые довольно трудно исследовать другими методами. Так, например, тиантрен Ci2H8S2 и соответствующие соединения селена и теллура имеют дипольные моменты, отличные от нуля, тогда как у феназина C12H8N2 момент равен нулю. [3]
Определение дипольного момента по измеренному изменению работы выхода при адсорбции требует знания природы адсорбционного процесса. Необходимо рассмотреть три вида адсорбции: а) ван-дер-ваальсову ( физическую) адсорбцию; б) ионную адсорбцию и в) ковалентную хемосорбцию. [4]
Определение дипольных моментов показало, что молекулы тех веществ, у которых можно предполагать отсутствие полярности, в действительности полярны. [5]
Определение дипольных моментов позволяет экспериментальным путем установить степень полярности данного ковалентного соединения. Из приведенных цифр видно, что азот, водород и хлор не имеют дипольных моментов. Этого и можно было ожидать, так как их молекулы симметричны. Молекулы хлороформа и метанола несимметричны и потому имеют дкпольные моменты. [6]
Определение дипольных моментов методом молекулярных пучков. [7]
Определение дипольных моментов проливает свет на эффекты сопряжения в других системах, помимо непредельных углеводородов и ароматических соединений. [8]
Определение дипольных моментов будет рассмотрено позднее, в разделе об электронных представлениях в органической химии ( стр. [9]
Определение дипольного момента с помощью эффекта Штарка дает значение ie, равное 0 72 дебая. Быстрое уменьшение штарковского расщепления с ростом J, как это видно из формулы (7.23), ограничивает точность измерений для сравнительно легких молекул, особенно при малом дипольном моменте. Например, на переходе J 0 - 1 были сделаны точные измерения для молекулы N2O [413], дипольный момент которой - оказался равным 0 166 дебая. [10]
Определение дипольного момента веществ проводится в очень разбавленных растворах путем экстраполяции на бесконечно разбавленные растворы. [11]
Определение дипольного момента комплекса по найденным таким образом значениям его поляризации требует, как показано выше, экстраполяции Рк к бесконечному разведению. [12]
Определение дипольного момента соединения может быть исполь -, зовано для решения различных структурных проблем. Суммарный дипольный момент молекулы зависит не только от числа и природы полярных групп ( связей), но и от их взаимного положения в молекуле. Так, молекулы углеводородов имеют небольшой дипольный момент ( меньше 0 5 Д) вследствие того, что моменты всех С - Н - связей почти одинаковы и в силу геометрии молекулы расположены так, что взаимно компенсируются. При замене одного из водородов в, углеводороде на заместитель, для которого дипольный момент связи углерод-заместитель ( или момент самой замещающей группы) заметно отличается от момента связи С - Н, молекула в целом становится полярной. [13]
Определение дипольных моментов тиофена п нескольких алкенов по методу Онзагера. [14]
Определение дипольных моментов комплексов металлов с я-аллильными лигандами во многих случаях дает ценную информацию о структуре этих комплексов, по крайней мере в растворе. Можно предположить, что в твердом состоянии эти комплексы, как и ( C3H5PdCl) 2, имеют вполне симметричную молекулярную структуру, но при растворении, очевидно, имеет место конформаци-онное изменение, возможно, со сдвигом мостиковых атомов галогенов. [15]
Страницы: 1 2 3 4