Зависимость - скорость - коррозия
Cтраница 2
 |
Зависимость скорости растворения стали от потенциала, который задавался электроду л-нитробен-зоатом гексаметиленимина ( 1 н. Na2S04. [16] |
Зависимость скорости коррозии от потенциала при внутренней поляризации нитробензоатом амина такая же, как и при внешней анодной поляризации: вначале при смещении потенциала в положительную сторону скорость растворения увеличивается. [17]
Зависимость скорости коррозии от концентрации кислорода носит линейный характер. При рН 10 критическая концентрация кислорода достигает значения, соответствующего насыщению воды воздухом ( 6 мл О2 / л), а для более щелочных растворов она ниже. [18]
Зависимость скорости коррозии от величины рН для разных металлов не одинакова. [19]
 |
Влияние концентрации растворенных газов на скорость коррозии меди в воде, г / ( ма-год. [20] |
Зависимости скорости коррозии меди от температуры воды при различных скоростях потока и содержания в ней кислорода и диоксида углерода приведены на рис. 11.3 и 11.4. Увеличение скорости движения воды увеличивает скорость коррозии за счет усиления доступа агрессивных газов, находящихся в воде, к поверхности меди. [21]
Зависимость скорости коррозии образцов из стали 12Х1МФ от содержания сероводорода в топочном газе при температуре 500 С показана на рис. 3.6. В интервале изменения концентрации H2S от 0 до 0 08 % в топочных газах, содержащих продукты химического недожога, скорость коррозии растет пропорционально концентрации сероводорода в газах. [22]
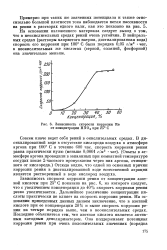 |
Зависимость скорости коррозии Re от концентрации HN03 при 25 С. [23] |
Зависимость скорости коррозии рения от концентрации азотной кислоты при 25 С показана на рис. 6, из которого следует, что с увеличением концентрации до 40 % скорость коррозии рения резко увеличивается. Дальнейшее увеличение концентрации кислоты практически не влияет на скорость коррозии рения. На основании приведенных данных делаем заключение, что в азотной кислоте при ее концентрации 20 % и выше скорость коррозии рения на четыре порядка выше, чем в не окислительных средах. Последнее объясняется тем, что азотная кислота является активным катодным деполяризатором. [24]
Зависимость скорости коррозии алюминия от величины рН раствора изучена Г. В. Акимовым и А. Они установили, что наименьшая коррозия алюминия наблюдается в нейтральных растворах ( рН5 - 9); при уменьшении, а также при увеличении значения рН скорость коррозии повышается. [25]
 |
Влияние концентрации растворенных газов на скорость коррозии меди в воде, г / ( м2 - год. [26] |
Зависимости скорости коррозии меди от температуры воды при различных скоростях потока и содержания в ней кислорода и диоксида углерода приведены на рис. 11.3 и 11.4. Увеличение скорости движения воды увеличивает скорость коррозии за счет усиления доступа агрессивных газов, находящихся в воде, к поверхности меди. [27]
Зависимость скорости коррозии алюминиевых сплавов от времени практически для всех сплавов имеет один и тот же характер. Первое время контакт металла с морской водой вызывает интенсивную коррозию, затем скорость коррозии постепенно уменьшается. Так, алюминиевый сплав 5052 интенсивно корродирует первые 15 - 17 сут, а затем наступает уменьшение скорости коррозии в связи с образованием на поверхности защитной пленки сложного состава, включающей продукты жизнедеятельности бактерий. [28]
Зависимость скорости коррозии алюминиевых сплавов or времени практически для всех сплавов имеет один и тот же характер. Первые несколько дней контакта сплава с морской водой протекает интенсивная коррозия, затем скорость коррозии постепенно уменьшается. [29]
Поэтому зависимость скорости коррозии от температуры для открытых питательных систем должна иметь точку максимума, определение которой приобретает практический интерес. [30]
Страницы: 1 2 3 4 5