Зависимость - скорость - коррозия
Cтраница 3
 |
Зависимость потенциала и истинной скорости коррозии стали в 0 1 н. Na2S04 от концентрации бората натрия. [31] |
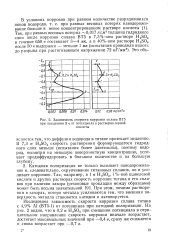
Такая зависимость скорости коррозии и потенциала от концентрации NaB03 отражается и на характере поляризационной кривой k ( ф) ( см. рис. 2 17): на участке активного растворения при незначительном смещении потенциала в положительную сторону наблюдается сильный рост скорости коррозии. Однако начиная с потенциала - - 0 35 В отмечается сильное падение скорости растворения. Поскольку пассивная часть электрода при этом не меняется в широкой области концентраций ингибитора, падение ч - ivvyjjvjCTK коррозии в активно-пасси Бнои Оиласти потенциалов обусловлено торможением анодной реакции. [32]
 |
Зависимость скорости коррозии сплава ВТ5. [33] |
Исследована зависимость скорости коррозии сплава титана с 4 9 % Al ( BT5 - 1) от потенциала при катодной поляризации. [34]
Определена зависимость скорости коррозии указанных сталей от концентрации спггртов и температуры. [35]
Отсутствие зависимости скорости коррозии от ширины зазора у таких малостойких сплавов, какими являются иеплакированные Д16 и В95, объясняется, по-видимому, уже тем обстоятельством, что скорость процесса начинает лимитироваться недостатком кислорода, а возможно и воды, в зазоре. [36]
Характер зависимости скорости коррозии от концентрации уротропина и влияния добавок уротропина на электродные потенциалы и кинетику электродных процессов дают возможность предположить, что в условиях службы выпарного аппарата уротропин является смешанным замедлителем коррозии. [37]
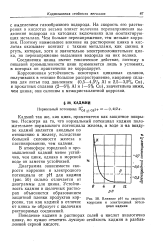 |
Влияние рН на скорость коррозии и электродный потенциал кадмия. [38] |
Диаграмма зависимости скорости коррозии и электродного потенциала от рН для кадмия ( рис. 50) сильно отличается от диаграммы для цинка. Устойчивость кадмия в щелочных растворах объясняется образованием защитной пленки продуктов коррозии, так как кадмий в отличие от цинка не образует с щелочами растворимых соединений. [39]
Кривая зависимости скорости коррозии от температуры в системе, сообщающейся с атмосферой, проходит через максимум, при 70 - 80 С. Это обусловлено увеличением коэффициента диффузии кислорода и уменьшением растворимости кислорода в воде при повышении температуры. [41]
Кривая зависимости скорости коррозии от температуры в системе, сообщающейся с атмосферой, проходит через максимум при температуре 70 - 80 С. Это обусловлено увеличением коэффициента диффузии кислорода и уменьшением растворимости кислорода при повышении температуры. [42]
Кривая зависимости скорости коррозии от температуры в системе, сообщающейся с атмосферой, проходит через максимум при 70 - 80 С. Это обусловлено увеличением коэффициента диффузии кислорода и уменьшением растворимости кислорода в воде при повышении температуры. [43]
Изучение зависимости скорости коррозии от потенциала методом химической пассивации показало, что на поляризационной кривой отсутствует участок активного растворения. При введении уже первых порций метаванадата натрия сталь находится на границе активно-пассивного состояния. Поскольку этот ингибитор л широкой области концентраций не изменяет площадь, на которой протекает анодная реакция растворения ( см. рис. 2 23), он не увеличивает эффективности катодного процесса. [44]
Отсутствие зависимости скорости коррозии от ширины зазора у таких малостойких сплавов, какими являются неплакированные Д16 и В95, объясняется, по-видимому, уже тем обстоятельством, что скорость процесса начинает лимитироваться недостатком кислорода, а возможно и воды, в зазоре. [45]
Страницы: 1 2 3 4 5
