Зависимость - скорость - коррозия - железо
Cтраница 1
Зависимость скорости коррозии железа и углеродистых сталей от концентрации солей в нейтральных растворах имеет вид кривой с максимумом вследствие уменьшения растворимости деполяризатора - кислорода при увеличении концентрации активирующих анионов. Установлено, что максимальная скорость коррозии наблюдается в 3 - 4 % - ных растворах хлоридов. [1]
Зависимость скорости коррозии железа от содержания растворенного кислорода носит линейный характер. [2]
Зависимость скорости коррозии железа и углеродистых сталей от концентрации хлоридов и сульфатов нейтральных растворов имеет вид кривых с максимумом ( см. рис. 242), зависящим от природы растворенной соли. С ростом концентрации солей увеличивается концентрация ионов хлора, сульфата и аммония, активирующих и облегчающих анодный процесс, и уменьшается растворимость деполяризатора кислорода ( см. рис. 162), что затрудняет протекание катодного процесса. В каком-то интервале концентраций сильнее сказывается первый эффект, а затем преобладает второй. [3]
Несомненно, что зависимость скорости коррозии железа в растворах солей от содержания кислорода имеет более сложный характер, так как роль кислорода двоякая: он усиливает коррозию в тех случаях, когда является деполяризатором, и уменьшает, когда пассивирует металл. Кроме того, в зависимости от неравномерного доступа кислорода к отдельным участкам металла могут образоваться гальванические пары, работающие по схеме концентрационных цепей. [4]
 |
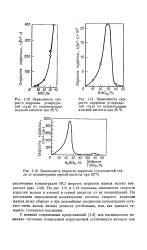
Зависимость скорости коррозии железа в воде от рН ( добавка HCI в кислой области и NaOH в щелочной области при двух температурах. [5] |
На рис. 30 представлена зависимость скорости коррозии железа от рН раствора. [6]
На рис. 17 представлена зависимость скорости коррозии железа от концентрации серной кислоты. [7]
На рис. 1.11 и 1.12 показаны зависимости скорости коррозии железа в азотной и серной кислотах от их концентраций. По достижении определенной концентрации кислоты скорость коррозии железа резко убывает и при дальнейшем увеличении концентрации остается очень малой, металл делается устойчивым, или, как принято говорить, становится пассивным. [9]
Зависимости скорости коррозии железа в раствораж оолей от содержания кислорода имеют сложный характер, тая как роль кислорода двоякая: он усиливает коррозию в тех случаях, когда является деполяризатором, и ослабляет коррозию, когда пассивирует металл. Кроме того, при неравномерном доступе кислорода на отдельных участках металла могут образоваться коррозионные гальванические пары. [10]
С уменьшением растворимости кислорода в большинстве случаев наблюдается снижение скорости коррозии железа. Зависимости скорости коррозии железа в растворах солей от содержания кислорода имеют сложный характер, так как роль кислорода двояка: он усиливает коррозию в тех случаях, когда является деполяризатором, и ослабляет коррозию, когда пассивирует металл. Кроме того, при неравномерном доступе кислорода на отдельных участках металла могут образовываться коррозионные гальванические пары. [11]
Эту концепцию подтверждают экспериментально установленные закономерности сероводородной коррозии. Отсюда становится понятной своеобразная зависимость скорости коррозии железа от содержания в среде сероводорода, если предположить, что контролирующей стадией коррозионного процесса является перенос реагирующих частиц через пленку сульфида железа. [12]
Для установления механизма коррозии стали в перемешиваемых электролитах было интересно проследить за зависимостью скорости коррозии этого металла от скорости вращения электрода или движения судна. На рис. 24 ( кривая 11) приведена зависимость скорости коррозии железа от скорости вращения электрода. Скорость коррозии железа выражена в мка / см2 и определена за первые 12 ч, когда влияние на нее вторичных факторов еще мало. Как видно, зависимость скорости коррозии железа от скорости вращения электрода носит тот же характер, что и для коррозионных элементов третьей группы. Таким образом, коррозия железа в интенсивно перемешиваемом ( при скоростях вращения электрода 200 об / мин и выше) нейтральном электролите, каким является морская вода, в значительной степени определяется скоростью реакции электрохимического восстановления кислорода. [13]
Для установления механизма коррозии стали в перемешиваемых электролитах было интересно проследить за зависимостью скорости коррозии этого металла от скорости вращения электрода или движения судна. На рис. 24 ( кривая 11) приведена зависимость скорости коррозии железа от скорости вращения электрода. Скорость коррозии железа выражена в мка / см5 и определена за первые 12 ч, когда влияние на нее вторичных факторов еще мало. Как видно, зависимость скорости коррозии железа от скорости вращения электрода носит тот же характер что и для коррозионных элементов третьей группы. Таким образом, коррозия железа в интенсивно перемешиваемом ( при скоростях вращения, электрода 200 об / мин и выше) нейтральном электролите, каким является морская вода, в значительной степени определяется скоростью реакции электрохимического восстановления кислорода. [14]
От рН зависит растворимость продуктов коррозии и, следовательно, возможность образования защитных пленок, состоящих из этих продуктов. К таким металлам относятся медь, хром, никель, кобальт. Зависимость скорости коррозии железа от рН при низких температурах подобна показанной на диаграмме рис. 1.9 6, а при высоких - на диаграмме рис. 1.9, а. Изменению рН соответствует изменение не только концентраций ионов Н и ОН -, но и других ионов, в частности аниона кислоты и катиона основания. Так как среди них могут быть ионы, оказывающие влияние на скорость коррозионных процессов, связывать изменение скорости коррозии только с изменением рН не всегда правильно. Необходимо учитывать влияние на скорость коррозии всех компонентов раствора электролита. [15]
Страницы: 1 2