Зависимость - скорость - коррозия - металл
Cтраница 1
Зависимость скорости коррозии металлов в растворах кислот не только от рН, но и от природы кислоты ( рис. 156) наталкивала исследователей на мысль о том, что анионы кислот принимают непосредственное участие в этом процессе, влияя на его скорость. [1]
Получены и экспериментально подтверждены зависимости скорости коррозии металлов от величины напряжений при упругих и упругопластических деформациях. Рассмотрены прочность и долговечность упругонагруженных труб в агрессивных средах, показано влияние схемы напряженного состояния на скорость механохимической коррозии и долговечность труб. Приведены экспериментальные данные по кинетике изменения напряжений и скорости коррозии. Даны расчеты предельной несущей способности и долговечности труб на основе исследований кинетики механохимического разрушения труб при упругопластических деформациях, подтвержденные экспериментально. [2]
Предложена математическая модель и зависимость скорости коррозии металла трубы от толщины слоя ГФГ в случае повреждения изоляции. Установлено, что слой ГФГ в 10 см снижает скорость коррозии на 40 %, по сравнению с засыпкой трубопровода обычным минеральным грунтом. Определено оптимальное значение толщины слоя ГФГ по критерию минимальных удельных затрат на проведение ремонтных работ. [3]
Основной при моделировании процессов коррозии является зависимость скорости коррозии металла от концентрации в электролите кислот, щелочей и других составляющих. При искусственных электролитах, которыми заполняется аналоговая модель, коррозия, как правило, протекает значительно быстрее, чем на трассе трубопровода. [5]
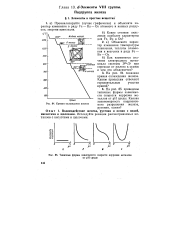 |
Типичные формы зависимости скорости коррозии металлов. [6] |
На рис. 85 приведены типичные формы зависимости скорости коррозии металлов от рН среды. [7]
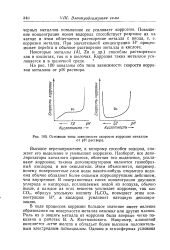 |
Основные типы зависимости скорости коррозии металлов от рН раствора. [8] |
На рис. 100 показаны оба типа зависимости скорости коррозии металлов от рН раствора. [9]
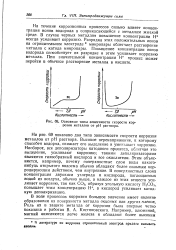 |
Основные типы зависимости скорости коррозии металлов от рН раствора. [10] |
На рис. 69 показано два типа зависимости скорости коррозии металлов от рН раствора. Высокое перенапряжение, к которому способен водород, снижает его выделение и уменьшает коррозию. Наоборот, все деполяризаторы катодного процесса, облегчая это выделение, усиливают коррозию; такими деполяризаторами являются газообразный кислород и все окислители. Этим объясняется, например, почему поверхностные слои воды какого-нибудь открытого водоема обычно обладают более сильным корродирующим действием, чем внутренние. В поверхностных слоях концентрация двуокиси углерода и кислорода, поглощаемых водой из воздуха, обычно выше, а каждое из этих веществ усиливает коррозию, так как СО2, образуя угольную кислоту Н СОз, повышает этим концентрацию Н, а кислород усиливает катодную деполяризацию. [11]
 |
Лабораторная установка для испытания химической стойкости материалов в бромистоводороднрй кислоте при 400 - 700 С. [12] |
В табл. 33 и на рис. 22 - 24 представлена зависимость скорости коррозии металлов и сплавов от времени в растворах бромистоводородной кислоты при 20 - 25 С. С повышением концентрации бромистоводородной кислоты коррозионная устойчивость металлических материалов снижается. [13]
Для вычисления защитного эффекта необходимо прежде всего получить кривую, выражающую зависимость скорости коррозии металла, который хотят защитить, от концентрации ингибитора в данной среде. [14]
Из изложенного выше следует, что при ускоренных испытаниях использовать повышение температуры можно, только учитывая зависимость скорости коррозии испытывающихся металлов от температуры. [15]
Страницы: 1 2
