Зависимость - скорость - окисление
Cтраница 1
Зависимость скорости окисления от температуры характеризуется временем ( в часах), которое при данной температуре необходимо затратить для достижения приблизительно одного и того же числа омыления. [1]
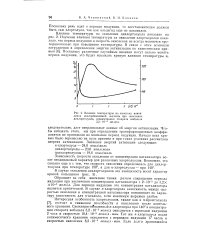 |
Влияние температуры на кинетику накопления дихлорбензойной кислоты при окислении дихлортолуола, концентрация стеарата кобальта 3 2 Ю-3 моль / л. [2] |
Зависимость скорости окисления от концентрации катализатора носит неодинаковый характер для различных хлортолуолов. [3]
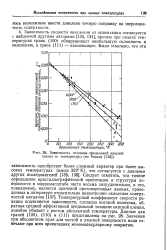 |
Зависимость толщины предельной окисной пленки or температуры ( по Родину. [4] |
Зависимость скорости окисления от ориентации согласуется с найденной другими авторами [133, 134], причем при низких температурах грань ( 100) обнаруживает наибольшую склонность к окислению, а грань ( 111) - наименьшую. [5]
Зависимость скорости окисления мотана от диаметра реактора при различных давлениях. [6]
Зависимость скорости окисления от природы органических загрязнений, находящихся в сточных водах, концентрации активного ила, адаптированного к данным органическим загрязнениям, количества кислорода, равномерно распределенного в аэротенке-смесителе, температуры сточных вод и активной реакции ( рН) сточных вод в приведенных ранее формулах не раскрыта. Между тем именно от совокупности всех этих условий зависят величина скорости окисления органических веществ в аэротенке-смесителе, необходимая продолжительность аэрации, удельный расход воздуха и а очистку 1 м3 сточных вод, а следовательно, необходимые строительные и эксплуатационные затраты. [7]
Зависимость скорости окисления от концентрации кислорода изучалась экспериментально, в частности Болландом [46], при окислении этиллинолеата, инициированном перекисью бензоила. [8]
Зависимость скорости окисления от концентрации инициатора определяется наклоном линии, полученной путем нанесения на график логарифма концентрации инициатора относительно логарифма скорости окисления. Явление автокатализа, имеющее место при окислении, обычно связывается с автоокислением. Автокатализ происходит вследствие неустойчивой природы образующейся перекиси. Перекись, возникающая в процессе окисления, подвергается в зависимости от ее свойств и условий реакции разложению. [9]
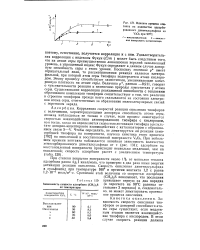 |
Влияние времени контакта на количество адсорбированного диметилсульфида на V2O5 при 90 С. [10] |
Зависимость скорости окисления тиоэфиров от донорной способности атома серы существует, если медленным этапом является взаимодействие тиоэфира с кислородом. [11]
Зависимость скорости окисления углеводородов от соотношения концентраций компонентов и изменение энергии активации связано, вероятно, с формированием лабильных комплексных соединений кобальта, в состав которых входит углеводород, 02, ацетат и бромид кобальта и вода. Образование комплекса значительно облегчается при температурах выше 85 С, когда под действием температуры начинается разрушение аква-комплексов. [12]
Зависимость скорости окисления кокса от закоксованности микросферического цеолитсодержащего катализатора, по данным [77], представлена на рис. 4.48. При содержании кокса на катализаторе более 1 % ( масс.) скорость его окисления изменяется незначительно. В интервале содержания кокса от 1 до 0 % ( масс.) скорость регенерации резко снижается и имеет наименьшее значение при выжиге остаточных количеств кокса. [13]
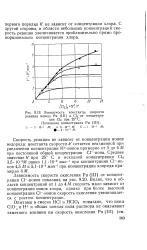 |
Зависимость константы скорости реакции между Ри ( III и С12 от концентрации С12 при 25 С. Начальная концентрация Ри ( III. [14] |
Зависимость скорости окисления Ри ( III) от концентрации С1 - - ионов показана на рис. 9.20. Видно, что в области концентраций от 1 до 4 М скорость мало зависит от концентрации ионов хлора, однако при более высокой концентрации С1 - - ионов скорость окисления увеличивается с ростом концентрации. [15]
Страницы: 1 2 3 4 5