Зависимость - скорость - процесс
Cтраница 1
Зависимость скорости процесса от корня квадратного из числа оборотов диска является, по-видимому, наи более надежным критерием, характеризующим механизм процесса и дополняемым характерными фигурами травления на поверхности диска. Вторым надежным критерием следует считать совпадение экспериментальной величины константы скорости реакции растворения с теоретической. [1]
Зависимость скорости процесса от концентрации реагентов содержит члены первого и второго порядка по концентрации формальдегида. [2]
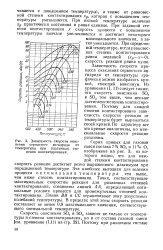
Зависимость скорости процесса от начальной концентрации серной кислоты, используемой для сульфирования сополимера ( рис. 5.32), показывает, что, чем ниже эта концентрация, тем при меньшей степени превращения устанавливается равновесие в системе. Причиной этого, как указывалось ранее, является гидратация сульфоионов, диффундирующих в гранулу сополимера. Гидратация приводит к деформации структуры жидкой среды в порах гранулы, которая выражается в уменьшении движущей силы процесса и установлении равновесия по воде. Сравнение экспериментальных и расчетных кривых кинетики сульфирования, представленных на том же рисунке, свидетельствует о существенном влиянии гидратации на установление межфазного равновесия в системе. [3]
 |
Зависимость скорости окисления сернистого ангидрида от температуры при различных степенях контактирования. [4] |
Зависимость скорости процесса окисления сернистого ангидрида от температуры графически можно изобразить кривой, имеющей максимум. Из уравнения ( I, 11) следует также, что скорость окисления SO2 в SO3 тем выше, чем меньше дсстигаемгястепень контактирования. [5]
 |
Угловые коэффициенты ( в В катодных ( - Ьк и анодных ( 6а поляризационных кривых при замедленной электрохимической стадии ( ак аа 0 5. t 25 С. [6] |
Из зависимости скорости процесса от потенциала может быть получена зависимость скорости от перенапряжения в более общем виде. Подставим в уравнение полной поляризационной кривой выражение для скорости процесса при равновесном потенциале и потенциале под током. [7]
Изучение зависимости скорости процесса ионного обмена от зернения сорбента часто позволяет однозначно ответить на вопрос: какая из стадий - химическая или диффузионная - ско-ростьопределяющая. Если скорость определяется химической реакцией двойного обмена, то кинетика процесса не зависит от размера зерна сорбента, и наоборот. Большинство данных по ионному обмену приводят к выводу, что определяющей практически всегда является диффузионная стадия. Исключение возможно для ионного обмена на низкоосновных катионитах или анионитах. Химическая кинетика может проявляться и в случае хроматографич. [8]
Изучение зависимости скорости процесса ионного обмена от зернения сорбента часто позволяет однозначно ответить на вопрос какая из стадий - химическая или диффузионная - ско-ростьопределяющая Если скорость определяется химической реакцией двойного обмена, то кинетика процесса не зависит от размера зерна сорбента, и наоборот Большинство данных по ионному обмену приводят к выводу, что определяющей практически всегда является диффузионная стадия Исключение возможно для ионного обмена на низкоосновных катионитах или анионитах Химическая кинетика может проявляться и в случае хроматографич. [9]
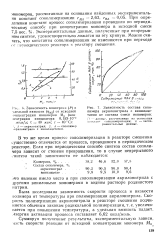 |
Зависимость состава сополимера акрилонитрила с винилацетатом от состава смеси мономеров. [10] |
Была исследована зависимость скорости процесса и вязкости полимера от температуры при полимеризации акрилонитрила. Скорость полимеризации акрилонитрила в реакторе смешения подчиняется обычным законам радикальной полимеризации т.е. увеличивается при повышении температуры, а удельная вязкость падает. Энергия активации процесса составляет 6 62 ккал / моль. [11]
Чаще наблюдается зависимость скоростей процесса от концентрации С2Н4 и 02 в дробных степенях. Темкин с сотрудниками [211] считает, что такое разнообразие в кинетических законах обусловлено различным содержанием кислорода в приповерхностном слое. [12]
 |
Схема потоков в двухсекционной противоточной установке непрерывного действия с движущимся слоем. [13] |
Только две зависимости скорости процесса рассматриваются в этом разделе. Первая ( в реакционно-кинетической форме) представлена из-за ее общей применимости, что было отмечено раньше. [14]
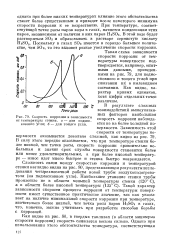 |
Скорость коррозии в зависимости от температуры стенки, а - для подмосковного угля. б - для тощего угля. [15] |
Страницы: 1 2 3 4