Зависимость - скорость - распад
Cтраница 1
Зависимость скорости распада от температуры не укладывается для твердого тэна в уравнение Аррениуса, возможно, вследствие изменения доли тэна, находящегося в жидком состоянии при различных температурах, из-за примесей или конденсированных продуктов распада, снижающих температуру плавления. [1]
 |
Зависимость скорости образования радикалов от концентрации гидроперекиси кумила. [2] |
Изучение зависимости скорости распада гидроперекиси кумила от концентрации продуктов окисления кумола - диметилфенил-карбинола, ацетофенона и бензойной кислоты - показало, что именно бензойная кислота ускоряет распад гидроперекиси на радикалы. [3]
Изучение зависимости скорости распада гидроперекиси купила от концентрации продуктов окисления кумола - диметилфенил-карбинола, ацетофенона и бензойной кислоты - показало, что именно бензойная кислота ускоряет распад гидроперекиси на радикалы. [4]
При исследовании зависимости скорости распада озона от навески катализатора была обнаружена начальная линейная зависимость участка скорости от величины навески. С увеличением навески свыше 30 мг наблюдается замедление скорости. [5]
Установлено, что зависимость скорости распада нестабилизированной перекиси водорода под действием - [ - излучения от интенсивности излучения достаточно хорошо описывается выражением v k I. Для истолкования установленных эффектов влияния полупроводников на возбуждение гетерогенных радиационно-химических реакций предложен механизм гетерогенной радиационно-химической сенсибилизации. [6]
При исследовании перекиси грег-бутила была также обнаружена зависимость скорости распада ее от растворителя. [7]
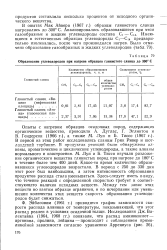 |
Образование углеводородов при нагреве образцов глинистого сланца до 300 С. [8] |
Эйблсоном ( 1961 г.) приводится график зависимости скорости распада аланина от температуры, показывающий, что этот распад реален в условиях осадочной толщи. [9]
Анализ продуктов распада транс-9 - декалилпероксифенилацетата ( XXII) и зависимость скорости распада от растворителя позволяют обнаружить такое изменение механизма при переходе от неполярного этилбензола к полярному ацетонитрилу. Об этой перемене механизма говорит также то, что при графическом сопоставлении значений gk с эмпирическим параметром полярности растворителей Ет ( см. раздел 7.3) получают разные наклоны корреляционных прямых для областей гомолитического и гетеролитического разложения. [10]
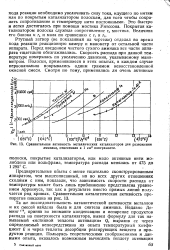 |
Сравнительная активность металлических катализаторов для разложения аммиака, отнесенная к 1 см2 поверхности. [11] |
Предварительные опыты с менее тщательно сконструированным аппаратом, чем вышеописанный, но во всех других отношениях сходным с ним, показали, что зависимость скорости распада от температуры может быть лишь приближенно представлена уравнением Аррениуса, так как в результате вместо прямых линий получается ряд кривых. [12]
Поскольку для квантовой модели среднее время жизни активной молекулы меньше, чем для классической, то, очевидно, теория Слейтера и в квантовом случае не может правильно передать зависимость скорости распада от давления. Никитин [15] показал, что квантовая статистическая теория распада может объяснить экспериментальную величину скорости распада N20 при низких давлениях, которая получается экстраполяцией экспериментальных данных к низким давлениям. Малая скорость активации означает фактически, что интерпретация скорости распада при промежуточных давлениях должна основываться на механизме ступенчатого возбуждения, а не на механизме сильных столкновений. [13]
Зависимость скорости распада п-гексана и л-октана от глубины реакции. [14]
Данные, полученные при изучении реакции гомогенного распада перекиси водорода под действием f - излучения, показали, что выход этой реакции в сотни раз больше выхода обычных ( не цепных) реакций; это заставляет принять цепной механизм радиационно-химического распада концентрированных растворов перекиси водорода. Установлена зависимость скорости радиациопно-химического распада перекиси водорода от температуры. [15]
Страницы: 1 2