Зависимость - скорость - распад
Cтраница 2
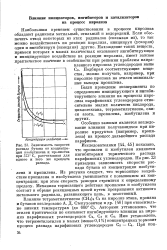 |
Зависимость скорости распада бутана от концентрации нзобутилена и пропилена при 573 С, рассчитанная для одного и того же процента распада. [16] |
Исследователями [44, 45] показано, что пропилен и изобутилен являются ингибиторами термического распада парафиновых углеводородов. На рис. 23 приведена зависимость скорости распада бутана от концентрации изобутилена и пропилена. Из рисунка следует, что тормозящее воздействие пропилена и изобутилена уменьшается с повышением их концентрации; при этом скорость реакции стремится к определенному пределу. Механизм тормозящего действия пропилена и изобутилена состоит в обрыве реакционных цепей путем превращения активного метильного радикала, развивающего цепь, в неактивный. [17]
Было установлено, что добавки изобутилена и пропилена оказывают тормозящее действие на скорость распада этана, пропана, бутана и изобу-тана, и в их действии наступает насыщение, соответствующее для данного углеводорода некоторой остаточной скорости w, независимой от природы добавки. В качестве примера см. рис. 1, на котором показана зависимость скорости распада пропана от концентрации добавок непредельных углеводородов. При этом добавки изобутилена при прочих равных условиях тормозят распад углеводородов сильное, чем добавки пропилена. Добавки дивинила и ацетилена не оказывают тормозящего действия на скорость распада углеводородов. [18]
Резкость излома связана не с клеткой, а с той довольно резкой зависимостью скорости распада радикалов от температуры по сравнению с их рекомбинацией. Скорость распада определяется суммой констант скоростей двух процессов: одна от температуры почти не зависит, а температурная зависимость другой описывается уравнением Аррениуса с энергией активации 20 - 25 ккал / моль. Большая величина энергии активации и определяет резкость излома. [19]
Первое направление реализуется для гидротриоксидов силанов. Кинетические и активационные параметры распада ( высокое отрицательное значение энтропии активации), значительный эффект заместителя, зависимость скорости распада от полярности растворителя, а также отсутствие влияния радикального ингибитора ионола на кинетику распада согласуются с преимущественно молекулярным ( 90 %) механизмом разложения. [20]
Недавно Винтер 229 произвел опыты над распадом аммиака на железе, применяя динамический метод, который дает возможность избежать многих неопределенностей, связанных с изучением этой реакции статическим методом. Винтер показал, что такая кинетическая зависимость получается в том случав, если наиболее медленной стадией реакции является удаление с поверхности атомов аэота, образующихся при распаде аммиака на поверхности железа. Интересно отметить, что для нескольких экспериментальных кривых, даваемых Винтером для зависимости скорости распада аммиака от парциального давления водорода при данной температуре и данном парциальном давлений аммиака, часть реакции происходила на катализаторе, присутсвующем еще в виде железа, а часть - уже тогда, когда значение A NH 2 / / DH давало возможность предполагать образование Fe4N, а в некоторых случаях даже и высшего нитрида. [21]
Страницы: 1 2