Определение - теплота - парообразование
Cтраница 3
 |
Изменение общей теплоты сгорания и зависимости от плотности и содержания инертных газон. [31] |
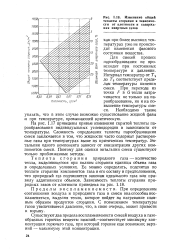
На рис. 1.17 приведена, кривые изменения скрытой теплоты парообразования индивидуальных углеводородов в зависимости от температуры Сложность определения теплоты парообразования смеси заключается в том, что жидкости часто содержат растворенные газы при температурах выше их критических температур. Энтальпия одного компонента зависит от концентрации других компонентов смеси. Поэтом для оценки энтальпии смеси существуют только приближенные методы. [32]
Циркуляционные приборы для изучения равновесия жидкость - пар были предложены И. Н. Бушмакиным ( см., например, [5157]), метод определения теплот парообразования разработал JVI. [33]
Как видно из уравнения ( 13), величина энтальпии парообразования Д по непосредственно связана с наклоном кривой зависимости давления пара от температуры. Для определения теплоты парообразования на осно ве уравнения Клапейрона-Клаузиуса ( 13) могут быть использованы различные выражения температурной зависимости давления пара. [34]
Как видно из уравнения ( 13), величина энтальпии парообразования Д / / по непосредственно связана с наклоном кривой зависимости давления пара от температуры. Для определения теплоты парообразования на осно ве уравнения Клапейрона - Клаузиуса ( 13) могут быть использованы различные выражения температурной зависимости давления пара. [35]
 |
Схема установки. [36] |
Используемая в данной работе установка основана на методе кипения. Для определения теплоты парообразования во время опыта к кипящей жидкости подводится некоторое измеряемое количество теплоты и определяется количество образовавшегося водяного пара. Влияние тепловых потерь в окружающую среду исключается способом проведения эксперимента. [37]
 |
Изменение общей теплоты сгорания в зависимости от плотности и содержания инертных газов. [38] |
На рис. 1.17 приведены кривые изменения скрытой теплоты парообразования индивидуальных углеводородов в зависимости от температуры. Сложность определения теплоты парообразования смеси заключается в том, что жидкости часто содержат растворенные газы при температурах выше их критических температур. Энтальпия одного компонента зависит от концентрации других компонентов смеси. Поэтому для оценки энтальпии смеси существуют только приближенные методы. [39]
Обе науки тесно связаны и взаимозависимы: Карно был инженером, интересовавшимся паровыми машинами, но то, что второй закон термодинамики широко применим во всех областях науки, показали Клаузиус, Кельвин, Максвелл и Гиббс. Уравнение Клаузиуса-Клапейрона, например, является исключительно полезным средством определения теплот парообразования по данным давлений паров, измерение которых значительно проще, чем самих теплот. [40]
Однако, несмотря на то, что эта корреляция является шагом вперед в решении сложной проблемы определения теплоты парообразования веществ с водородными связями, лучшие результаты дают другие методы, представленные в разделах III. [41]
Приведенная температура 298 15 / Тс при этом существенно изменяется от вещества к веществу, принимая, например, в ряду н-парафинов значения от 0 976 для этана до 0 389 для н-эйкозана. В связи с этим для расчета параметра растворимости широкого круга веществ по уравнению / I / необходимо располагать эффективными методиками определения теплоты парообразования и плотности жидкой фазы индивидуальных веществ во всем диапазоне температур сосуществования фаз. [42]
В комплексе термодинамических характеристик энтальпии испарения и сублимации занимают особое место, так как позволяют оценивать термодинамические свойства вещества в различных его состояниях, связывать термодинамические свойства с кинетическими константами, сопоставлять энергию связи и изменения энергетических характеристик со структурой вещества. Между тем измерение энтальпии парообразования, особенно энтальпии сублимации, является сложной экспериментальной задачей и одним из наименее разработанных разделов экспериментальной термодинамики. Действительно, в научной литературе не рассмотрены в достаточной мере состояние и возможности экспериментальной техники по определению теплот парообразования и давления насыщенного пара органических веществ. [43]
Страницы: 1 2 3