Определение - эквивалентная точка
Cтраница 2
Так как значение рН при определении эквивалентной точки титрования низкое ( растворителем используется даже уксусная кислота [16]), то карбоновые кислоты определению кетонов и альдегидов не мешают. [16]
В кулонометрическом титровании применяются различные способы определения эквивалентной точки. [17]
Мастер должен показать учащимся приемы титрования и определения эквивалентной точки. Нужно напомнить учащимся, что реакция диазотирования, лежащая в основе этого метода анализа, - взаимодействие азотистой кислоты с ароматическим амином, - для различных аминов протекает с различной скоростью. Для ускорения реакции в ряде случаев добавляют бромистый калий. Большое значение имеет и скорость титрования. В зависимости от природы определяемого амина выбирают температуру реакции и скорость прибавления раствора азотистокислого натрия. В случае медленно диазотирующихся аминов прибавление раствора азотистокислого натрия ведут медленно. Как и в прямом бромометрическом титровании, здесь применяется внешний индикатор. [18]
Из перечисленных в табл. 11.2 индикаторов для определения эквивалентной точки пригодны лишь крезоловый красный и фенолфталеин. Чем слабее кислота, тем менее отчетлива эквивалентная точка, тем более узок интервал значений рН и менее надежен способ титрования. [19]
Принцип действия титрометра основан на потенциометрическом методе определения эквивалентной точки при титровании исследуемой среды раствором щелочи. Конструкция прибора допускает разбавление в случае необходимости исследуемой среды каким-либо растворителем. В частности, при использовании прибора для контроля процесса этерификации в производстве диоктилфталата контролируемый продукт разбавляют этиловым или метиловым спиртом. [20]
Электрод, которым пользуются при потенциометрическом титровании для определения эквивалентной точки, носит название индикаторного. [21]
Электрод, которым пользуются при потенциометрическом титровании для определения эквивалентной точки, носит название индикаторного. [22]
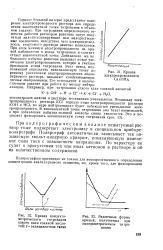 |
Кривая кондукто-метрического титрования едкого кали соляной кислотой. У-эквивалентная течка.| Различные формы кривых, получаемых при амперометрическом титровании. [23] |
Гораздо больший интерес представляет измерение электропроводности раствора для определения эквивалентной точки титрования в объемном анализе. При титровании определяемого вещества рабочим раствором реактива могут получаться малодиссоциирующие или малорастворимые соединения, вследствие чего электропроводность титруемого раствора заметно понижается. При этом минимум электропроводности на кривой наблюдается в конце титрования и соответствует эквивалентной точке. Добавление же не большого избытка реактива вызывает новое увеличение электропроводности, которое и считают признаком конца титрования. Этот метод, позволяющий определить эквивалентную точку по резкому увеличению электропроводности анализируемого раствора, называют кондуктометри-ческим титрованием. Его используют в количественном анализе при работе по методу нейтрализации. [24]
Экстрагентом служил метиловый спирт, а оптимальным способом определения эквивалентной точки оказался электрометрический. Была разработана установка для размола зерна ( длительность измельчения навески 5 г составляет 2 - 2 5 мин); экстракции воды ( длительность 10 мин) и отбора пробы экстракта; конструкция установки преследует цель исключения потерь влаги в ходе перечисленных операций. [25]
Для установления небольших количеств ароматических-аминов применен фотометрический метод определения эквивалентной точки при прямом титровании 0 001 М раствором уксусного ангидрида в безводном пиридине. Эквивалентную точку находят по исчеЫовению поглощения исходного ароматического амина. [26]
Метод основан на титровании влаги реактивом Фишера с электриметрическим определением эквивалентной точки. [27]
Электрод, которым пользуются при потенциометр ическом титровании для определения эквивалентной точки, носит название индикаторного. В зависимости от того, является ли электрод обратимым по отношению к ионам титруемого вещества или по отношению к ионам реагента, потенциал его по мере титрования согласно уравнению ( 1) будет соответственно уменьшаться или увеличиваться. В начале титрования потенциал индикаторного электрода изменяется медленно, но вблизи эквивалентной точки, уже при прибавлении незначительного количества реагента ( 1 - 2 капли), его потенциал изменяется скачком. Этот скачок потенциала индикаторного электрода и дает возможность определить эквивалентную точку. [28]
Наибольший интерес представляет измерение электропроводности в объемном анализе для определения эквивалентной точки при титровании. [29]
Мастер производственного обучения должен показать учащимся приемы титрования и определения эквивалентной точки. Нужно напомнить им, что реакция диазотирования, лежащая в основе этого метода анализа - взаимодействие азотистой кислоты с ароматическим амином - для различным аминов протекает с различной скоростью. Дня ускорения реакции в ряде случаев добавляют бромид калия. Большое значение имеет и скорость титрования. В зависимости от природы определяемого амина выбирают температуру реакции и скорость прибавления раствора нитрита натрия. В случае медленно диазотирующихся аминов раствор азо-тистокислого натрия прибавляют медленно. Как и в прямом бромометрическом титровании, здесь применяется внешний индикатор. [30]
Страницы: 1 2 3 4