Определение - фторид-ион
Cтраница 2
Существуют два основных метода определения фторид-ионов при содержании их в воде порядка 10 - 4 %: спектрофотометриче-ский и потенциометрический с использованием ионоселективного электрода с мембраной из фторида лантана. В случае потенцио-метрического метода посторонние ионы в значительно меньшей степени мешают определению фторид-иона, и этот метод обычно используют для анализа питьевой воды без ее предварительной обработки. В этом случае для удаления из воды катионов путем замены их на Н используют сильнокислотную катионооб-менную смолу. [16]
В настоящее время распространены методы определения фторид-ионов, основанные на их свойстве связывать ионы многовалентных металлов циркония, тория, титана, железа ( III) в очень устойчивые комплексные анионы. В анализируемый раствор вводят окрашенные соединения указанных металлов; фторид-ионы, связывая эти металлы в бесцветные комплексы, вызывают ослаб ление окраски пропорционально своей концентрации в растворе, и по ослаблению окраски рассчитывают их содержание. Поскольку такое ослабление окраски происходит и под действием других ионов, часто присутствующих в природных и сточных водах, например сульфат - и фосфат-ионов, в большинстве случаев определение фторид-ионов требует предварительной их отгонки из рас, твора ( см. разд. [17]
Все применявшиеся до последнего времени методы определения фторид-ионов основаны на их свойстве связывать ионы многовалентных металлов [ циркония, тория, титана, железа ( III) ] в очень устойчивые комплексные анионы. В анализируемый раствор вводятся окрашенные соединения указанных выше металлов; фторид-ионы, связывая эти металлы в бесцветные комплексы, вызывают ослабление окраски пропорционально своей концентрации в растворе, и по ослаблению окраски рассчитывают их содержание. Поскольку такое ослабление окраски происходит и под действием других ионов, часто присутствующих в природных и сточных водах, например, сульфат - и фосфат-ионов, в большинстве случаев определение фторид-ионов требует предварительной их отгонки из раствора ( см. разд. [18]
Известно, что наиболее распространенный метод определения фторид-иона в растворе - ториметрическое титрование - может давать ошибки, выходящие за пределы, принятые в элементном анализе. Эти ошибки обусловлены трудностью визуальной индикации окраски в точке эквивалентности. [19]
Можно ли практически использовать осаждаемую форму Сар2 при определении фторид-ионов. [20]
В водно-спиртовой среде ( 80 % спирта) возможно определение фторид-ионов в количествах до 4 мкг. [21]
Известно большое число весовых, объемных и колориметрических методов определения фторид-ионов в растворах после минерализации. В большинстве способов нужно предварительно отделять мешающие определению, сопутствующие ионы, особенно фосфат-ионы, образующиеся при минерализации фторфосфорных соединений. Фосфат-ионы не мешают определению фтор-иона при осаждении его в виде хлорфторида или бромфторида свинца, количество которых можно определять как весовыми50, так и объемными способами. Вследствие сравнительно большой растворимости PbCIF точность весового определения мала. Более трудоемким способом определения фтора в присутствии фосфатов является осаждение его при рН 4 0 - 4 5 в виде фторида кальция 5б, добавленный избыток кальция определяют комплексометрически. Однако в этих способах приходится отделять фтор от фосфат-ионов. К перегоняемой смеси для связывания галоидоводородных кислот добавляют сульфат серебра, сероводород связывают серебряной спиралью, находящейся в ловушке, помещенной по пути следования пара. Разработаны различные типы перегонных аппаратов, из которых прибор Питцка и Эрлиха59 имеет то преимущество, что при работе с ним не нужно наблюдать за процессом отгонки, так как требуемая для образования пара вода находится в цикле. Отгонку ведут из раствора, содержащего серную и хлорную кислоты. Кроме того, к смеси добавляют немного битого стекла, для того чтобы фтор отгонялся в виде кремнефтористоводородной кислоты. Последняя поглощается в приемнике со слабым раствором карбоната натрия. [22]
Реакция образования разнолигандного комплекса перспективна в аналитическом плане для разработки прямого фотометрического метода определения фторид-иона. [23]
При использовании метода стандартных добавок для анализа чая, в котором может содержаться до 17000 мкг / г алюминия, было найдено [141], что присутствие алюминия ( и железа) приводит к значительным ошибкам определения фторид-ионов. Использование цитрата натрия в качестве маскирующего агента приводит к количественному выделению фторида из комплексов с алюминием, железом, магнием и кремнием. [24]
Определение фторид-ионов в минералах проводится с целью их идентификации. [25]
Определение фторид-ионов в присутствии бора осложнено образованием фто-роборатов, к которым не чувствителен фторид-селективный электрод. Чтобы исключить возможность образования фторобо-ратов, образцы сжигают, предварительно подобрав соответствующие условия. Раствор образца впрыскивают в водородно-кис-лородное пламя и собирают продукты горения в ловушку с 1 М раствором NaOH. Концентрацию фторид-ионов в образце либо определяют непосредственно, применяя микропроцессорный иономер lonalyzer ( модель № 901), либо рассчитывают по калибровочному графику. [26]
Определение фторид-ионов в сахарном тростнике проводят с тем, чтобы установить, не загрязняют ли заводы, выплавляющие алюминий, расположенные вблизи от них плантации. [27]
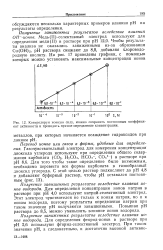 |
Контролируя ионную силу, можно сохранять постоянным коэффициент активности и проводить прямое определение концентрации. [28] |
Для определения фторид-ионов в растворе при рН 2 6 используют фторид-селективный электрод. [29]
Определению мешает свободный хлор, его можно восстановить, добавляя ОД) 5 мл 0 5 % - ного раствора ар-сенита натрия на каждую 0 1 мг свободного хлора. При определении фторид-ионов в концентрации 1 мг / л возникает ошибка, равная 0 1 мг / л в присутствии 1800 мг / л хлорид-ионов, 0 2 мг / л алюминия, 5 мг / л железа ( III), 5 мг / л фосфат-ионов или 1 мг / л гекса-метафосфата натрия. [30]
Страницы: 1 2 3 4