Определение - термодинамическая функция
Cтраница 3
И дело здесь не в том, что не известен еще способ измерения, а в том, что процесс образования отдельных ионов из простых веществ ( Na из Na и С1 - из СЬ) в принципе не реализуем, поскольку в таком процессе нарушается закон сохранения заряда. Поэтому для определения термодинамических функций образования ионов перечень простых веществ, в котором каждый элемент представлен олсой нейтральной химической формой, необходимо дополнить хотя бы одной заряженной формой какого-либо элемента. [31]
В настоящей книге сначала излагаются общие закономерности термодинамики и их применение к химии, точнее к изучению химических равновесий в классическом плане. Затем рассказывается о статистических методах определения термодинамических функций с использованием результатов-квантовой механики. Завершают книгу две главы о растворах и правиле фаз, также составленные в основном классическом аспекте, и, наконец, глава о применении термодинамики к неравновесным процессам. [32]
В настоящей книге сначала излагаются общие закономерности термодинамики и их применение к химии, точнее к изучению химических равновесий в классическом плане. Затем рассказывается о статистических методах определения термодинамических функций с использованием результатов квантовой механики. Завершают книгу две главы о растворах и правиле фаз, также составленные в основном классическом аспекте, и, наконец, глава о применении термодинамики к неравновесным процессам. [33]
В настоящей книге сначала излагаются общие закономерности термодинамики и их применение к химии, точнее к изучению химических равновесий в классическом плане. Затем рассказывается о статистических методах определения термодинамических функций с использованием результатов квантовой механики. Завершают книгу две главы о растворах и правиле фаз, также составленные в основном классическом аспекте и, наконец, глава о неравновесных процессах. [34]
Проведен расчет термодинамических характеристик систем в областях гомогенности и равновесного сосуществования жидкой и твердой фаз. Предложен способ оценки ожидаемых ошибок определения конечных термодинамических функций при применении метода Сторонкина - Шульца. Введена функция, характеризующая интенсивность процессов комплексообразования в тройных растворах. Проведена количественная оценка избыточной свободной энергии автокомплексообразования и взаимодействия солевых компонентов исследуемых систем. Показана взаимная согласованность полученных результатов. [35]
В [74] в рамках метода частичных функций распределения получено выражение для внутренней энергии плазмы водорода, отличающееся меньшей поправкой на неидеальность, по сравнению с теорией Дебая. Проводится сравнение с экспериментом по определению термодинамических функций плазмы цезия. В работе [76] некулоновский вид электрон-ионного взаимодействия на малых расстояниях объясняется влиянием электронных оболочек иона. Расчет термодинамических параметров классической системы выполнен на основе метода функциональных интегралов. [36]
Применение эксергетического метода к анализу нефтехимических установок связано с определением эксергии потоков углеводородов, нефтяных фракций и их смесей в газообразном и жидком состояниях. Из-за сложного характера смесей и необходимости определения термодинамических функций во многих точках технологических схеа при разных температурах и давлениях практика расчетов требует привлечения вычислительной техники. [37]
Современная теория теплоемкостей базируется на квантовой теории и на анализе молекулярных и атомарных спектров. Анализ этих спектров дает необходимые данные для определения термодинамических функций различных веществ и их тепло-емкостей. [38]
В практике расчетов термодинамических величин эти трудности обходят путем различного рода ограничения статистических сумм на основе тех или иных физических соображений. Последовательный, но более сложный подход к определению термодинамических функций основан на физической модели, где рассматриваются ядра и электроны, а куло-новское взаимодействие между ними учитывается на основе квантовой и статистической теории. При этом вклады в термодинамические функции от непрерывного и дискретного спектров возникают одновременно и являются конечными. [40]
В качестве примера обратимой реакции, используемой для определения термодинамических функций и протекающей в гальваническом элементе, состоящем из водородного и хингидрон-ного электродов, рассмотрим восстановлелие хинона в гидрохинон. [41]
Квантово-статистический метод расчета констант равновесия является единственно возможным при высоких температурах, когда нельзя прибегать к термохимическим измерениям. Кроме того, он является и более точным, чем все другие методы определения термодинамических функций. [42]
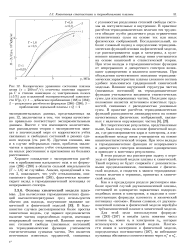
Компоненты смеси кубового остатка предварительно разделяли на неполярной колонке со скваланом. При 40 была получена хроматограмма ( см. рисунок), из которой видно присутствие в смеси, по крайней мере, 10 компонентов. Для определения термодинамических функций растворения были определены относительные объемы удерживания основных компонентов смеси при различных температурах. Для этого выходящий из колонки пик улавливали ловушкой, погруженной в жидкий азот, и при помощи шестиходового крана вводили в хроматограф Хром-1 с колонкой, заполненной одной из полярных неподвижных фаз. [43]
Точность определения разных величин может колебаться в широких пределах. Она зависит от применяемого метода, от тщательности проведения измерений и от чистоты вещества. Так, статистические методы определения термодинамических функций веществ могут быть применены в разном приближении. При исполь - зовании модели жесткий ротатор - гармонический осциллятор игнорируется возможность изменения межатомных расстояний при усилении вращения молекулы с повышением температуры, а также усиление при этом ангармоничности колебаний. В более точных методах расчета достигается возможность учета в той или другой степени этих осложнений, что особенно важно для высоких температур. [44]
Точность определения разных величин может колебаться в широких пределах. Она зависит от применяемого метода, от тщательности проведения измерений и от чистоты вещества. Так, статистические методы определения термодинамических функций веществ могут быть применены в разном приближении. При использовании модели жесткий ротатор - гармонический осциллятор игнорируется возможность изменения межатомных расстояний при усилении вращения молекулы с повышением температуры, а также усиление при этом ангармоничности колебаний. В более точных методах расчета достигается возможность учета в той или другой степени этих осложнений, что особенно важно для высоких темлератур. [45]
Страницы: 1 2 3 4