Зависимость - начальная скорость - реакция
Cтраница 2
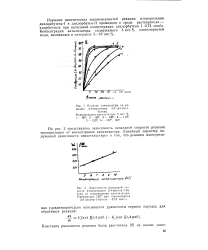 |
Влияние температуры на ре -. акцию изомеризации 3 4-дихлор - 1. [16] |
На рис. 2 представлена зависимость начальной скорости реакции изомеризации от концентрации катализатора. [17]
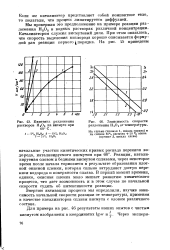 |
Кинетика разложения растворов HSOS на висмуте при.| Зависимость скорости разложения Н2О2 от температуры. [18] |
Энергию активации процесса мы определили, изучив зависимость начальной скорости реакции от температуры, применяя в качестве катализаторов сплавы висмута с оловом различного состава. [19]
 |
Кривая уравнения Михаэли-са - Ментен. гиперболическая зависимость начальных скоростей катализируемой ферментом реакции от концентрации субстрата. [20] |
Пользоваться графиком, построенным в прямых координатах зависимости начальной скорости реакции v0 от начальной концентрации субстрата [ SJ, неудобно, поскольку максимальная скорость Vmai является в данном случае асимптотической величиной и определяется недостаточно точно. [21]
 |
Калибровочные кривые для систем, подчиняющихся закономерности. начальная еюсь рость Л [ С ] ис1 5 ( текст. [22] |
Как показано на рис. 12.3, при построении зависимости начальной скорости реакции от концентрации катализатора получается прямая линия с наклоном А, отсекающая на оси ординат отрезок В. [23]
Для определения порядка реакции по метакриловой кислоте были получены зависимости начальных скоростей реакции от исходной концентрации кислоты. Тангенс угла наклона прямой в логарифмических координатах lgW0 - lg GOMAK, равный нулю ( рис. 1 а), показывает, что взаимодействие окиси этилена с метакриловой кислотой не зависит от концентрации последней. [24]
В случае односубстратной реакции задача сводится к получению серии данных, характеризующих зависимость начальной скорости реакции от концентрации субстрата, и к соответствующей графической обработке этих данных. [25]
Конкурентное ингибирование проще всего можно распознать экспериментальным путем, определив влияние концентрации ингибитора на зависимость начальной скорости реакции от концентрации субстрата. Для выяснения вопроса о том, по какому типу-конкурентному или неконкурентному-происходит обратимое ингибирование фермента ( дополнение 9 - 3), весьма удобно преобразовать уравнение Михаэлиса-Ментен в линейную форму. Чаще всего для этой цели используют метод двойных обратных величин. [27]
Концентрации добавки и реагентов были близки. Зависимости начальной скорости реакции в замороженных растворах в бензоле и диоксане от концентрации нитробензола и циклогексана изображены на рис. 8.9. При концентрации нитробензола 0 3 М скорость реакции достигает максимального значения. [29]
 |
Константы Михаэлиса для некоторых ферментов. [30] |
Страницы: 1 2 3

