Зависимость - начальная скорость - реакция
Cтраница 3
Еще более сложный вид имеют ур-ння кинетики двухсубстратных ферментативных реакций, в особенности обратимых реакций, в к-рых фермент-субстратные комплексы претерпевают многостадийные превращения. Однако в значительном числе случаев, исследуя зависимость начальной скорости реакции от концентрации субстрата, оказывается возможным вычислить основные кпнетич. Нетрудно видеть, что эта величина представляет собой молекулярную активность фермента. Величина константы Михаэлиса даже для простейших ферментативных реакций более сложна для интерпретации, поскольку определяется соотношением трех констант скорости. Кт представляет константу диссоциации комплекса ES на Е и S, к-рая в ферментативной кинетике наз. Константа субстрата служит мерой сродства фермента к субстрату ( сродство обратно пропорционально величине A s) и, следовательно, является важной мерой каталитич. [31]
Однако в настоящее время обнаружено много ферментов, у которых зависимость начальной скорости реакции от концентрации субстрата описывается не гиперболой, а сигмоидной кривой, и мы, несомненно, обязаны рассмотреть теоретические основы этого явления. [32]
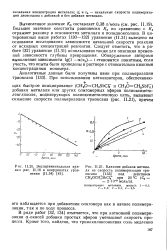 |
Влияние добавок метилаля на скорость полимеризации триоксана под действием CH3OCHjSbCle при 20 С ( С0 2 - 10 - 3 моль / л. [33] |
Большее значение константы равновесия К2 по сравнению с / d отражает разницу в основностях метилаля и полидиоксолана. В цитированных выше работах [130-132] уравнение (11.31) выведено на основании исследования зависимости начальной скорости реакции от исходных концентраций реагентов. Следует отметить, что в работе [32] уравнение (11.31) использовано также для описания временной зависимости глубины превращения. Обнаруженное авторами выполнение зависимости lg ( l - - а / ар) - t становится понятным, если учесть, что опыты были проведены в растворе с относительно низкими концентрациями мономера. [34]
Расчетные уравнения и графики для определения начальных скоростей реакций и механизма их протекания для приведенных выше случаев представлены на рис. V-17. В соответствии с рис. V-17 в табл. V-ба - V-15 указаны определяющие стадии процесса для девяти основных случаев, которые могут встретиться на практике при определении зависимости начальной скорости реакции от общего давления в системе. [35]
 |
Кинетические кривые для бимолекулярной реакции с участием промежуточного вещества для первого ( а и второго ( б набора констант скоростей. [36] |
Для записи решения удобно использовать самописец. При определении формального порядка по исходным веществам и эффективной константы скорости реакции ( а) записывают кинетические кривые при нескольких начальных концентрациях [ А ] 0) если [ В ] о const, и строят зависимость начальной скорости реакции ш0 от [ А ] 0 в логарифмических координатах. [37]
 |
Кинетические кривые для бимолекулярной реакции с участием промежуточного вещества для первого ( а и второго ( б набора констант скоростей. [38] |
Для записи решения удобно использовать самописец. При определении формального порядка по исходным веществам и эффективной константы скорости реакции ( а) записывают кинетические кривые при нескольких начальных концентрациях [ А ] 0, если [ В ] 0 const, и строят зависимость начальной скорости реакции WQ от [ А ] 0 в логарифмических координатах. В соответствии с уравнением скорости о о эфф ( [ А ] огп [ В ] ог или гу0 § 1гЭфф т § [ А ] о п lgi [ B ] 0) где т и п - порядки реакции по веществам А и В, строят в координатах Igay0 - lg [ A ] o прямую, из тангенса угла наклона которой находят порядок реакции по веществу А. [39]
Для выяснения этого фактора памп изучены кинетические закономерности реакции эпоксидирования октадиена-1 7 гидропсроксидом третичного бутила. Температура варьировалась от 70 до 100 С, количество катализатора - резината молибдена составляло 6 - 10 4 моль Мо / л, концентрации октадиена-1 7 и ГПТБ изменялись соответственно от 0 5 до 2 8 и от 0 15 до 1 5 моль / л за счет изменения содержания растворителя - толуола. Представленные на рис. 1 зависимости начальной скорости реакции от концентрации ГПТБ, октадиена-1 7 и катализатора характеризуют первый порядок реакции по каждому компоненту. С увеличением концентрации реагентов скорость реакции стремится к некоторому пределу: максимальной скорости, что типично для реакций, протекающих через образование промежуточного комплекса. В случае ( рис. 1 в) загиб кинетической кривой отражает образование ассоциированных форм катализатора, которые образуются при увеличении концентрации последнего. [40]
Страницы: 1 2 3