Определение - энергия - активация
Cтраница 1
Определение энергии активации весьма важно как для оценки свойств ферментов, так и для оценки каталитических процессов - оно имеет общебиологическое значение. Установлено, что ферменты, ускоряющие одну и ту же реакцию, снижают энергию активации по-разному, если были выделены из одинаковых органов разных животных или из разных тканей животного одного вида. Интересно, что изменения активности в зависимости от температуры различны у разных растений. [1]
Определение энергии активации в - диффузионной области методом быстрого изменения температуры опыта иллюстрирует рис. 38, на котором представлены получаемые описанным путем температурные зависимости скорости реакции в координатах уравнения Аррениуса. [3]
Определение энергии активации из температурного коэфициента скорости реакции ( § 353) дает в полном согласии с этой величиной: 0 44400 кал. [4]
Определение энергии активации, как мы видели, приводит к значениям, заниженным в два раза. Зависимость от давления может быть найдена корректно при условии, что ее определение производится в начальной стадии реакции или же методом выделения ( гл. [5]
Определение энергии активации для ван-дер-ваальсовых жидкостей не представляет сложностей, так как зависимость In D / ( 1 / Г) линейна. Для водородосвязанных жидкостей эта зависимость нелинейна, что создает определенные трудности при определении энергии активации. В этом случае применяется [68] линейно-кусочная аппроксимация, предполагая, что в пределах выбранных участков предэкспонента и энергия активации остаются постоянными. Справедливость такого подхода была проверена на воде. [6]
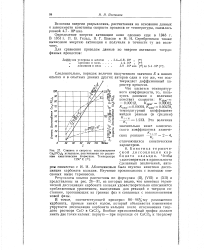 |
Степень и скорость восстановления. [7] |
Определение энергии активации нами сделано еще в 1948 г. В 1951 г. П. В. Гельд, В. Г. Власов и Н. Н. Серебреников также вычислили энергию активации и получили в точности ту же величину. [8]
Определения энергии активации произведены, исходя из фиг. [9]
Определение энергии активации процесса полимеризации необходимо проводить в присутствии катализатора, состав и актив-иость которого во времени остаются неизменными. [10]
Определение энергии активации реакций углерода с газами проводилось неоднократно. Однако величины энергии активации часто неправильно интерпретировались. [11]
Определение энергии активации радикальной реакции экспериментальным путем требует проведения исследуемой реакции в чистом виде без затемнения ее другими реакциями, что является трудным, но возможным. [12]
Определения энергий активации прямых и обратных процессов показали, что энтальпия образования окта-фторциклобутана из двух молекул тетрафторэтилена равняется - 50 кк. Эта величина значительно больше, чем величина - 25 ккал, которая, как полагают [44], отвечает образованию циклобутана из двух молекул этилена, и она показывает, что в тетрафторэтилене имеется слабая двойная связь и ( или) имеется благоприятное расположение атомов фтора и прочные одинарные связи в октафторциклобутане. [13]
Для определения энергии активации часто пользуются уравнением Аррениуса4, которое связывает константу скорости реакции с температурой. [14]
Страницы: 1 2 3 4