Зависимость - степень - диссоциация
Cтраница 1
Зависимость степени диссоциации от строения молекул растворенного вещества легко проследить для однотипных молекул, образующих электролит. [1]
Зависимость степени диссоциации от концентрации раствора можно определить, применяя к процессу электролитической диссоциации общие закономерности, полученные для обратимых химических реакций ( гл. [2]
Зависимость степени диссоциации от концентрации затрудняет использование этой величины для сравнения большого числа электролитов, так как не всегда можно иметь растворы выбранной концентрации. [3]
Зависимость степени диссоциации СО2 от температуры приведена на фиг. [4]
 |
Сопоставление молекулярных констант и степени диссоциации для 0 1 н. раствора галогеноводородов. [5] |
Зависимость степени диссоциации от строения молекул растворенного вещества легко проследить для однотипных молекул, образующих электролит. [6]
Зависимость степени диссоциации от концентрации раствора можно определить, применяя к процессу электролитической диссоциации общие закономерности, полученные для обратимых химических реакций ( гл. [7]
Зависимость степени диссоциации слабого электролита от разведения раствора также наглядно можно показать, используя тот факт, что при равновесии скорости прямого и обратного процесса равны и равновесные концентрации находятся в простом соотношении со степенью диссоциации. [8]
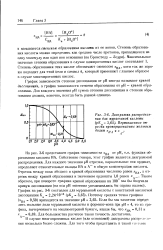 |
Диаграмма распределения для муравьиной кислоты ( рКа 3 65. Вертикальные отрезки пропорциональны мольным долям х. [9] |
График зависимости степени диссоциации от рН иногда называют кривой диссоциации, а график зависимости степени образования от рН - кривой образования. Для каждого значения рН сумма степени диссоциации и степени образования должна, конечно, всегда быть равной единице. [10]
Оно выражает зависимость степени диссоциации от концентрации электролита. [11]
Оно выражает зависимость степени диссоциации от концентрации электролита. [12]
Уравнение (2.74) выражает зависимость степени диссоциации от концентрации раствора. [13]
Уравнение (9.10) выражает зависимость степени диссоциации от концентрации раствора. [14]
Это уравнение и выражает зависимость степени диссоциации йодистого водорода от температуры. [15]
Страницы: 1 2 3