Зависимость - степень - конверсия
Cтраница 1
Зависимость степени конверсии NH3 от времени катализа и температуры: а - давление 10 at на 20 сетках; б - давление 20 ат на 30 сетках. [1]
Зависимость степени конверсии от объемной скорости газа для различных катализаторов устанавливают обычно экспериментально. [2]
Изучены зависимости степени конверсии хлорорганических растворителей от давления паров, продолжительности реакции, температуры, содержания платины в катализаторе. [3]
 |
Зависимость степени конверсии от времени - в присутствии катализатора и без него ( обозначения даны в тексте. [4] |
Определение зависимости степени конверсии от времени и сравнение предельной величины, полученной этим путем, с равновесным значением для тех же условий ( температура и давление), позволяют судить об эффективности данного процесса. Так, на рис. 4 представлены два варианта зависимости степени конверсии от времени и отмечена равновесная термодинамически возможная конверсия. Кривая / характеризует случай, когда термодинамическая равновесная конверсия практически может быть достигнута лишь в течение неопределенно длительного времени, тогда как кривая 2 показывает, что при благоприятных условиях ( например, в присутствии катализатора) достигается конверсия, равная термодинамически возможной в более короткое время, и дальнейшее увеличение времени реакции уже не приведет к увеличению конверсии. [5]
Определение зависимости степени конверсии от времени и сравнение предельной величины, полученной этим путем, с равновесным значением для тех же условий ( температура и давление), позволяют судить об эффективности данного процесса. Так, на рис. 4 представлены два варианта зависимости степени конверсии от времени и отмечена равновесная термодинамически возможная конверсия. Кривая / характеризует случай, когда термодинамическая равновесная конверсия практически может быть достигнута лишь в течение неопределенно длительного времени, тогда как кривая 2 показывает, что при благоприятных условиях ( например, в присутствии катализатора) достигается конверсия, раь-ная термодинамически возможной в более короткое время, и дальнейшее увеличение времени реакции уже не приведет к увеличению конверсии. [6]
Были определены зависимости степени конверсии от времени контакта при различных составах паро-газовой смеси. Полученные результаты подтвердили правильность кинетического уравнения первого порядка относительно окиси углерода. [7]
 |
Константы скорости и энергии активации окислительной дегидродимеризации олефинов.| Кинетика окисления бензола. [8] |
Рассчитан по зависимости степени конверсии от времени контакта. [9]
Экспериментальное подтверждение зависимости степени конверсии как от реакционного объема, так и от высоты аппарата было получено Пруденом и Вебером [35] на трехфазной системе. [10]
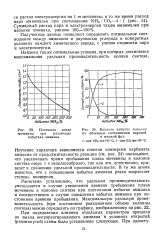 |
Влияние избытка аммиака на объемные соотношения паровой. [11] |
Изучение характера зависимости степени конверсии карбамата аммония от продолжительности реакции ( см. рис. 24) показывает, что увеличивать время пребывания плава мочевины в колонне синтеза сверх 1 ч нецелесообразно, так как это, естественно, приведет к снижению удельной производительности. В то же время известно, что с повышением избытка аммиака резко возрастает степень конверсии. [12]
Опытные данные представлены зависимостью степени конверсии метана от объемной скорости при атмосферном давлении. Как видно из рис. III.22, в температурном интервале 750 - 850 СС изменение объемной скорости от 1000 до 5000 ч 1 практически не сказывается на конверсии метана, а последняя близка к равновесной. [13]
На рис. Х-2 приведена зависимость степени конверсии от температуры в непрерывных реакторах двух типов для трех значений отношения V [ F. При этом используются данные рис. Х-1. Из рис. Х-2 следует, что при одинаковых условиях реактор идеального вытеснения обеспечивает более высокую степень превращения, чем реактор идеального смешения. [14]
На рис. 46 приведены зависимости степени конверсии от безразмерного времени tkit при различных начальных концентрациях фермента. [15]
Страницы: 1 2 3 4