Зависимость - температура - кристаллизация
Cтраница 1
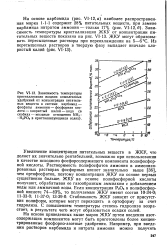
Зависимость температуры кристаллизации ЖКУ от концентрации питательных веществ показана на рис. VI-13. ЖКУ могут образовывать пересыщенные растворы при переохлаждении на 5 - 6 С. [2]
Изучение зависимости температуры кристаллизации ( плавления) от состава системы составляет сущность термического анализа. Диаграммы, построенные по данным термического анализа температура кристаллизации - состав, называются фазовыми диаграммами плавкости. Определение количества твердых фаз, образующихся при остывании расплавов заданного состава, осуществляется на основе фазовых диаграмм плавкости по правилу рычага или правилу отрезков. [3]
Кривая OFGH описывает зависимость температуры кристаллизации чистой воды от давления. Кривая А С ( см. рис. 22) описывает зависимость давления насыщенных паров чистого газа гид-ратообразователя ( С2Нв) от температуры. Равновесная кривая зависимости температуры образования гидрата от давления состоит из характерных отрезков кривой, наклон которых определяется термодинамическими условиями и фазовым состоянием компонентов. Кривая АВ определяет условия существования гидрата этана при t 0 С, когда гидрат образуется из паров этана и воды, находящейся в состоянии льда. [4]
Для полного суждения о зависимости температуры кристаллизации растворов и расплавов от их состава, результаты относящихся сюда измерений удобно представлять в виде особых диаграмм плавкости. При построении таких диаграмм для смеси двух компонент ( веществ) А и В, на оси абсцисс откладывается количество каждой из этих компонент, выраженное в процентах ко всему составу, а на оси ординат - температура кристаллизации. [5]
 |
Фазовое равновесие жидкость-пар в системе гексаметилендиамин-гексаметиленимин 7. [6] |
В табл. 40 приведены зависимости температуры кристаллизации бинарных смесей гексаметилендиамин - е-аминокапронитрил и гексаметилендиамин - 1 2 - диаминоциклогексан24 в пределах концентраций гексаметилендиамина 92 - 98 8 мол. Обе системы в исследуемом интервале концентраций образуют твердые растворы. [7]
Основным условием при использовании зависимости температуры кристаллизации от степени кристаллизации ( доли жидкой фазы) для расчета содержания примесей является строгое постоянство скорости кристаллизации в течение всего процесса кристаллизации. Только при этом условии время кристаллизации может быть использовано для определения доли жидкой фазы. [8]
Найти выражение для расчета зависимости температуры кристаллизации от концентрации ( 377ЗЛ) равн для кристаллизации вещества из идеального раствора. [9]
На рис. 15.10 показан характер зависимости температуры кристаллизации раствора, образованного двумя различными веществами А и В, от концентрации в нем вещества В. [10]
Раздел физико-химического анализа, посвященный изучению зависимости температуры кристаллизации или плавления исследуемой системы от ее состава, называется термическим анализом. Объектами термического анализа Служат самые разнообразные вещества: металлы, органические соединения, соли и др. Данные термического анализа оформляются в виде диаграммы плавкости. Экспериментально систему А-В изучают во всем интервале концентраций от чистого компонента А до чистого компонента В. [11]
А и 0 %) - Сплошная кривая выражает собою зависимость температуры кристаллизации сплава от его состава, а пунктирная - температуры плавления кристаллов от их состава. Эти кривые показывают, с одной стороны, что при одном и том же составе жидкости и кристаллов, жидкость будет кристаллизоваться при - иной температуре ( в данном случае при более высокой чем кристалл плавиться. [12]
Для исследования металлических систем важное4 значение имеет раздел физико-химического анализа, изучающий зависимость температуры кристаллизации ( или плавления) от состава системы и называемый термическим анализом. [13]
Изучены диаграммы плавкости двойных систем: НаО - моноэти-ленглвколь, НгО - диэтиленгликоль, Н2О - триэтиленгликоль и зависимость температуры кристаллизации льда от добавки полигликолей. [14]
Для веществ, которые удовлетворяют только что описанным условиям, можно определить содержание примеси даже в том случае, если не известна температура кристаллизации абсолютно чистого вещества, при условии, что может быть измерена зависимость температуры кристаллизации от величины закристаллизовавшейся фракции. Если концентрация примеси мала и температура кристаллизации понижается пропорционально содержанию примеси, то разница между начальной температурой кристаллизации и температурой кристаллизации, когда закристаллизовалась половина образца, равняется понижению, соответствующему количеству примеси в начальном образце. Таким образом, концентрация примеси может быть рассчитана, если известно понижение температуры кристаллизации, соответствующее присутствию 1 мол. [15]
Страницы: 1 2 3