Экспериментальное определение - константа - равновесие
Cтраница 1
Экспериментальное определение констант равновесия с достаточно высокой степенью точности является делом весьма непростым. [1]
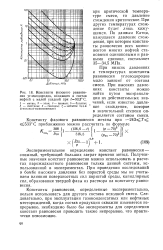 |
Константы фазового равновесия углеводородов, входящих в состав нефтей с малой усадкой при. 93 3 С. [2] |
Экспериментальное определение констант равновесия - сложный, требующий больших затрат времени метод. [3]
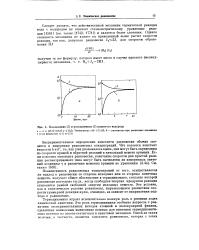 |
Накопление ( 1 и расходование ( 2 йодистого водорода. [4] |
Экспериментальное определение константы равновесия обычно сводится к измерению равновесных концентраций. Что касается констант скорости / си fe, то, как уже указывалось выше, они могут быть определены из скорости прямой и обратной реакций в начальный момент времени. [5]
Экспериментальное определение константы равновесия обычно сводится к измерению равновесных концентраций. Что касается констант скорости прямой и обратной реакций, то, как уже указывалось выше ( стр. Кроме того, если известна константа равновесия, константы скорости могут быть вычислены из измеренных значений величины х в различные моменты времени. [6]
Методы экспериментального определения констант равновесия основаны на анализе состава реакционной смеси после достижения ею состояния химического равновесия. Только совпадение ( в пределах ошибки опыта) аналитических данных по составу реакционной массы может в этом случае гарантировать, что изучается истинное равновесие. Основные экспериментальные приемы для измерения констант равновесия делятся на две группы: 1) статические методы; 2) динамические методы. [7]
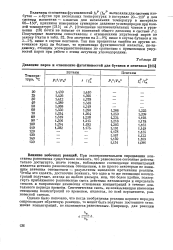 |
Давление паров и отношение фугативностей для бутанов и пентанов. [8] |
При экспериментальном определении константы равновесия существенно показать, что равновесное состояние действительно достигнуто, иначе говоря, наблюдаемое соотношение концентраций является истинно равновесным отношением, а не просто некоторым не имеющим значения отношением - результатом неполного протекания реакции. Чтобы это сделать, достаточно показать, что одно и то же отношение концентраций получают, исходя из любого изомера, или, что более удобно, подвергнуть приближенно равновесную смесь действию катализатора и определить степень и направление изменения отношения концентраций в течение длительного периода времени. Синтетическая смесь, не показывающая изменение отношения концентраций со временем, является, но всей вероятности, равновесной смесью. [9]
 |
Равновесные концентрации метанола. [10] |
Поэтому результаты экспериментального определения константы равновесия реакции синтеза метанола не могут служить надежной основой для проведения термодинамических расчетов. [11]
Методы расчета и экспериментальное определение констант равновесия в системах аминокислота - ионит. [12]
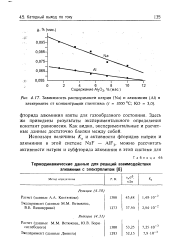 |
Зависимость растворимости натрия ( Na и алюминия ( А1 в электролите от концентрации глинозема ( / 1000 С. КО 3 0. [13] |
Здесь же приведены результаты экспериментального определения констант равновесия. Как видно, экспериментальные и расчетные данные достаточно близки между собой. [14]
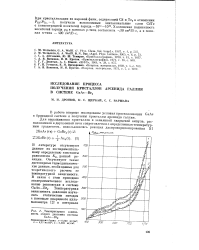 |
Температурная зависимость общего давления системы GaAs - Вг2. [15] |
Страницы: 1 2