Экспериментальное определение - константа - равновесие
Cтраница 2
В литературе отсутствуют данные по экспериментальному определению константы равновесия Kft данной реакции. Отсутствуют также достоверные термодинамические данные, необходимые для теоретического расчета ее температурной зависимости. [16]
Однако имеются реакции, для которых экспериментальное определение констант равновесия или очень сложно, или совсем неосуществимо. [17]
Расчеты химических равновесий имеют большое значение, так как экспериментальное определение константы равновесия может быть сопряжено с большими трудностями ( высокие температуры или давления, медленные реакции, нарушение равновесия процессом измерения и др.) - Практическое значение таких расчетов связано с нахождением направления протекания реакций, выхода продуктов и соответствующих энергетических эффектов. [18]
В 1967 г. Элленридер, Кастелана и Шумахер [157] повторили экспериментальное определение константы равновесия диссоциации тетрафторгидразина. [19]
 |
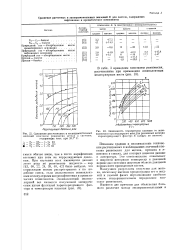
Константы равновесия процесса диссоциации водорода. [20] |
Совпадение между наблюдаемыми и вычисленными значениями вполне удовлетворительное, если принять во внимание трудности экспериментального определения константы равновесия процесса диссоциации водорода. Вычисленные значения являются, вероятно, более надежными, так как известно, что функции распределения и теплота диссоциации, использованные при расчете, являются точными. [21]
 |
Изменение свободной энергии в реакции цис-буген-2. тра. нс-бутен-2. [22] |
Хотя в уравнении ( 11) константа равновесия дана как отношение фу-тативностей, тем не менее экспериментальное определение константы равновесия не дает непосредственно величину этого отношения. Не практикуется также и экспериментальное определение парциального давления каждого из компонентов в равновесной смеси. Аналитические методы в общем случае могут дать только величины, выражающие количество ( весовое или объемное) каждого компонента в данном образце. Из этих величин может быть найдено отношение концентраций, чаще - отношение молярных долей NetNa изомеров в равновесной смеси для данных условий эксперимента. Из этого отношения должно быть найдено или рассчитано отношение фугативностей при помощи дополнительных данных. Способ расчета зависит от того, проводилась изомеризация в газовой или в жидкой фазе. [23]
Наилучшие результаты получены для метана, поскольку высокие концентрации его в жидкой и газовой фазах обусловливают наиболее точное экспериментальное определение констант равновесия. [25]
По-видимому, существуют два основных обстоятельства, обусловливающих ограниченность констант ионного обмена для многих изученных систем: не всегда достаточно надежна воспроизводимость показателей у ионообменных сорбентов заводского нтем более укрупненного лабораторного изготовления и довольно значительны, особенно с учетом коэффициентов активности, трудности определения названных величин. Действительно, экспериментальное определение констант равновесия сводится к длительному ( до достижения равновесия) контактированию смолы с раствором, отделению смолы от раствора и определению концентрации компонентов в фазах. На первый взгляд кажется, что в силу эквивалентности обмена можно ограничиться определением при данной температуре не четырех ( две - в смоляной фазе и две - в растворе) равновесных концентраций компонентов, а лишь одной, например, равновесной концентрации вытесняемого лона в растворе. Все остальные концентрации могут быть в принципе найдены расчетным путем: эквивалентная равновесная концентрация вытесняемого иона в смоле равна разности между полной обменной емкостью и концентрацией вытесняемого иона в растворе, равновесную концентрацию вытесняющего иона рассчитывают по разности между его исходным и сорбированным количествами. [26]
Для этого достаточно иметь возможность экспериментального определения константы равновесия рассматриваемой реакции при двух различных температурах. [27]
Единственное, что для этого необходимо - это представить соответствующую реакцию в виде суммы полуреакций. Если известны значения стандартных потенциалов, то расчет можно провести так же, как и в двух предыдущих примерах. Однако если необходимые стандартные потенциалы неизвестны, то можно составить гальванический элемент, пригодный для экспериментального определения констант равновесия. [28]
Страницы: 1 2