Экспериментальное определение - коэффициент - активность
Cтраница 1
Экспериментальное определение коэффициентов активности, названных эффектами среды, производится при том же ионном составе, при котором определяются коэффициенты активности в воде. Таким образом, произведение тун тух - ( X - одновалентный анион) и отношение mYH / mYMe е - одновалентный катион) так же, как отношения mYCI - / mYx - и YH Л / Лл Для слабых кислот НА или НА и YHA или т мх для незаряженных частиц являются термодинамически определенными величинами. [1]
Экспериментальное определение коэффициентов активности, названных эффектами среды, производится при том же ионном составе, при котором определяются коэффициенты активности в воде. Таким образом, произведение тун тух - ( X - одновалентный анион) и отношение mYH / mYMe ( Me - одновалентный катион) так же, как отношения mYcr / mYx - и YH Л / ЛА для слабых кислот НА или НА и YHA или т мх Для незаряженных частиц являются термодинамически определенными величинами. [2]
Экспериментальное определение коэффициентов активности всех участников равновесия ионной ассоциации в растворе не всегда возможно. [3]
Принципиальные трудности экспериментального определения коэффициентов активности отдельных ионов следуют из того факта, что в растворе всегда присутствуют по меньшей мере два вида противоположно заряженных ионов. [4]
Тем не менее сложность экспериментального определения коэффициентов активности для каждого случая вынуждает прибегать к подобному способу, так как без применения коэффициентов активности расчет по одним лишь аналитическим концентрациям повлек бы к несравненно большим погрешностям. [5]
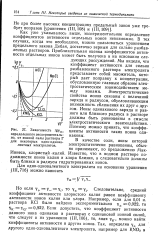 |
Зависимость lgY, определенного экспериментально, от ионной силы раствора Г для некоторых, одно-одновалентных электролитов. [6] |
Как уже указывалось выше, экспериментальное определение коэффициентов активности отдельных ионов невозможно. В тех случаях, когда это необходимо, можно пользоваться уравнением предельного закона Дебая, достаточно верным для сильно разбавленных растворов. Приблизительная оценка коэффициентов активности отдельных ионов может быть получена и на основании следующих рассуждений. Мы видели, что коэффициент активности для сильно разбавленного раствора электролита представляет собой множитель, который дает поправку к концентрации, обусловленную главным образом электростатическим взаимодействием между ионами. Электростатические свойства ионов связаны с величиной заряда и радиусом, обусловливающим возможность сближения их друг с другом. Ионы одинакового заряда и равного или близкого радиуса в растворе должны быть равноценны в смысле электростатического взаимодействия. Поэтому можно принять, что коэффициенты активности таких ионов одинаковы. [7]
Как уже указывалось выше, экспериментальное определение коэффициентов активности отдельных ионов невозможно. В тех случаях, когда это необходимо, можно пользоваться уравнением предельного закона Дебая, достаточно верным для сильно разбавленных растворов. [8]
В настоящее время имеются трудности в экспериментальном определении коэффициентов активности ионов, а отсюда и самой активности. [9]
В заключение нужно отметить, что наиболее точный способ экспериментального определения коэффициентов активности основан на измерении электродвижущих сил гальванических элементов. Этот способ будет, рассмотрен в гл. [10]
В заключение нужно отметить, что наиболее точный способ экспериментального определения коэффициентов активности основан на измерении электродвижущих сил гальванических элементов. Этот способ будет рассмотрен в гл. [11]
Так как характер сил межионного взаимодействия может меняться в зависимости от состояния электролита, экспериментальное определение коэффициентов активности производится только в растворах, находящихся в равновесном состоянии. [12]
Константы равновесия, полученные в предположении идеальной жидкой фазы, являются неточными. Необходимо экспериментальное определение коэффициентов активности, причем полученные данные следует обрабатывать таким образом, чтобы иметь возможность рассчитывать коэффициенты активности как функцию состава жидкой фазы. Известные уравнения Вооля и Редлиха - Кистера для многокомпонентных систем приемлемы для машинного расчета. [13]
Этим методом определяют коэффициент активности электролита в целом, а не отдельных его ионов. Метод экспериментального определения коэффициентов активности отдельных ионов еще не разработан. Поэтому измеряют коэффициент активности электролита в целом, рассчитывают его активность и затем путем различных допущений оценивают активности ионов. [14]
Поэтому практически расчет эффективных констант экстракции часто вызывает трудности и в настоящее время константы рассчитаны только для нескольких сотен экстракционных систем, в то время как число таких систем, описанное в литературе, превышает 10 тысяч и про должает неуклонно увеличиваться. Наиболее распространенный способ экспериментального определения коэффициентов активности необходимых для расчета экстракционных равновесий заключается в следующем. [15]
Страницы: 1 2